题目内容
下列溶液中有关物质的浓度关系正确的是( )
| A、c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl) |
| B、等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
考点:离子浓度大小的比较
专题:
分析:A、c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中NH4HSO4电离出的氢离子抑制铵根离子水解;
B、根据物料守恒,碳与氯元素在溶液中存在的所有微粒浓度相等;
C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液呈酸性,c(Na+)<c(CH3COO-);
D、电荷守恒分析解答.
B、根据物料守恒,碳与氯元素在溶液中存在的所有微粒浓度相等;
C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液呈酸性,c(Na+)<c(CH3COO-);
D、电荷守恒分析解答.
解答:
解:A、NH4HSO4电离出的氢离子抑制铵根离子水解,c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中,c[(NH4)2SO4]<c(NH4HSO4)<c(NH4Cl),故A错误;
B、根据物料守恒,碳与氯元素在溶液中存在的所有微粒浓度相等,所以c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-),故B正确;
C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液呈酸性,c(Na+)<c(CH3COO-),故C错误;
D、在二元弱酸的酸式盐NaHA溶液中,根据电荷守恒可以c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),故D错误;
故选B.
B、根据物料守恒,碳与氯元素在溶液中存在的所有微粒浓度相等,所以c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-),故B正确;
C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液呈酸性,c(Na+)<c(CH3COO-),故C错误;
D、在二元弱酸的酸式盐NaHA溶液中,根据电荷守恒可以c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),故D错误;
故选B.
点评:本题考查了电解质溶液中离子浓度大小比较,电荷守恒分析,盐类水解的理解应用,注意溶液稀释过程中离子浓度变化分析,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
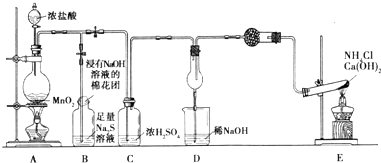
下列装置所示的实验,能达到实验目的是( )
A、 分离碘酒中碘和酒精 |
B、 实验室制NH3 |
C、 除去Cl2 中的HCl |
D、 排水法收集NO |
下列说法或表达正确的是( )
| A、乙醇、糖类和蛋白质都是人体必需的营养物质 |
B、NH4I的电子式: |
| C、石油是混合物,其分馏产品汽油也是混合物 |
| D、陶瓷、水晶、水泥、玻璃都属于硅酸盐 |
 下表中各组物质之间不能通过一步反应实现下图转化的是( )
下表中各组物质之间不能通过一步反应实现下图转化的是( )| 甲 | 乙 | 丙 | |
| A | AlCl3 | Al(OH)3 | Al2O3 |
| B | SiO2 | H2SiO3 | Na2SiO3 |
| C | Cl2 | HCl | NaCl |
| D | CH2=CH2 | CH3CH2Cl | CH3CH2OH |
| A、A | B、B | C、C | D、D |
把0.05molNaOH固体分别加入下列100mL液体中,溶液的导电能力变化不大的是( )
| A、0.5mol/LHF(弱酸) |
| B、0.5mol/L盐酸 |
| C、0.5mol/L.醋酸 |
| D、自来水 |
下列叙述正确的是( )
| A、胶体和溶液的本质区别是能否发生丁达尔效应 |
| B、酸性氧化物不一定是非金属氧化物,而碱性氧化物一定是金属氧化物 |
| C、离子键只存在于离子化合物中,共价键只存在于共价化合物中 |
| D、强电解质与弱电解质的分类依据是电解质水溶液导电能力的强弱 |
常用的抗生素“先锋Ⅵ”为粉末状固体,每瓶含“先锋Ⅵ”0.5g,注射时应配成质量分数大约为20%的溶液,则使用时每瓶大约需加入蒸馏水(水的密度近似为 1g/cm3)( )
| A、2ml | B、3ml |
| C、4ml | D、5ml |