题目内容
8.下列离子方程式不正确的是( )| A. | H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H+十SO42-→BaSO4↓+2H2O | |
| B. | CuSO4溶液与NaOH溶液反应:Cu2++2OH-→Cu(OH)2↓ | |
| C. | NaOH溶液中通入少量CO2:2OH-+CO2→CO32-+H2O | |
| D. | CH3COOH溶液与NaOH溶液反应:H++OH-→H2O |
分析 A.二者反应生成硫酸钡和水;
B.二者反应生成氢氧化铜沉淀和硫酸钠;
C.二氧化碳少量反应生成碳酸钠和水;
D.醋酸为弱酸应保留化学式.
解答 解:A.H2SO4与Ba(OH)2溶液反应,离子方程式:Ba2++2OH-+2H+十SO42-→BaSO4↓+2H2O,故B正确;
B.CuSO4溶液与NaOH溶液反应,离子方程式:Cu2++2OH-→Cu(OH)2↓,故C正确;
C.NaOH溶液中通入少量CO2,离子方程式:2OH-+CO2→CO32-+H2O,故C正确;
D.CH3COOH溶液与NaOH溶液反应,离子方程式:CH3COOH+OH-→H2O+CH3COO-,故D错误;
故选:D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
18.如图所示Mg-H2O2电池以海水为电解质溶液,下列说法正确的是( ) 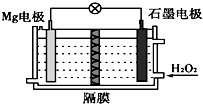

| A. | Mg 电极是该电池的正极 | B. | H2O2 在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的pH 增大 | D. | 溶液中Cl-向正极移动 |
16.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下11.2 L甲烷含有2NA个共价键 | |
| B. | 4.8 g Mg和氯气反应得到电子数为0.4 NA个 | |
| C. | 0.1 mol•L-1的氢氧化钠溶液中含钠离子数为0.1NA个 | |
| D. | 5.6 g铁与足量的稀硫酸反应失去电子数为0.3NA个 |
3.下列说法正确的是( )
| A. | 16O2、18O2互为同位素 | B. | H2O、D2O、T2O的化学性质不同 | ||
| C. | 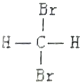 和 和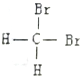 是两种不同结构 是两种不同结构 | D. | 白磷与红磷互为同素异形体 |
6.只用一种试剂,可区别Na2SO4、NH4Cl、MgSO4四种溶液,这种试剂是( )
| A. | HCl | B. | BaCl2 | C. | AgNO3 | D. | NaOH |
3.下列化学方程式或离子方程式正确的是( )
| A. | 过量的NaOH与Ca(HCO3)2反应:2OH-+Ca2++2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| C. | 乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH-→CH3COOH+C2H5O- | |
| D. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+=2Fe3++3H2O |
4.实验室制取氯化氢,有关叙述正确的是( )
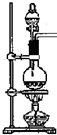

| A. | 利用浓硫酸的吸水性和氧化性 | |
| B. | 开始制备气体时应先加热后向烧瓶中加硫酸 | |
| C. | 利用浓硫酸的难挥发性和酸性 | |
| D. | 组装完实验装置立即加试剂、加热制气体 |
 如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.将镁片加入小试管内,然后注入足量的盐酸,请根据要求完成下列问题:
如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.将镁片加入小试管内,然后注入足量的盐酸,请根据要求完成下列问题: