题目内容
14.下列属于碱性氧化物的是( )| A. | Ca(OH)2 | B. | Na2O | C. | SiO2 | D. | H2SO4 |
分析 能与酸反应生成盐和水的氧化物为碱性氧化物,且只含金属元素、氧元素两种元素,一般为金属氧化物,但某些金属氧化物(Mn2O7、Al2O3)不是碱性氧化物,以此来解答.
解答 解:A.Ca(OH)2含Ca、O、H三种元素,属于碱,故A错误;
B.Na2O和酸反应生成盐和水属于碱性氧化物,故B正确;
C.SiO2 和碱溶液反应生成盐和水,属于酸性氧化物,故C错误;
D.H2SO4 属于酸,不是氧化物,故D错误;
故选B.
点评 本题考查物质的分类,为基础性习题,把握物质的组成、碱性氧化物的判断等为解答的关键,侧重分析与应用能力的考查,注意概念的理解及应用,题目难度不大.

练习册系列答案
相关题目
4.已知还原性:I->Fe2+>Br-.向含有Cl-、Fe2+、Br-、I-各0.1mol (其余为Na+)的溶液中通入标准状况下的氯气,通入氯气的体积和相关离子的物质的量的关系正确的是( )
| A. | 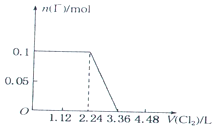 | B. | 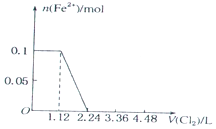 | ||
| C. | 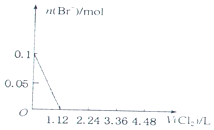 | D. | 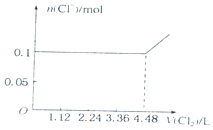 |
5.下列说法中正确的是( )
| A. | 1molOH-的质量为17g•mol-1 | |
| B. | 0.5mol H2所占体积约为11.2L | |
| C. | 等质量的金刚石和晶体硅所含原子个数之比为7:3 | |
| D. | 1mol NaCl固体溶于0.5L水中,所得溶液的物质的量浓度为2mol•L-1 |
2.绿色能源是指使用过程中不排放或排放极少污染物的能源.下列属于绿色能源的是( )
①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材 ⑦地热能.
①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材 ⑦地热能.
| A. | ①②③⑤ | B. | ②④⑤⑥ | C. | ③④⑤⑦ | D. | ①②⑤⑦ |
9.下列鉴别物质或离子的方法能达到目的是( )
| A. | 用氨水鉴别MgCl2溶液和AlCl3溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 用AgNO3鉴别Na2CO3溶液和NaCl溶液 | |
| D. | 用足量的盐酸和BaCl2溶液鉴别溶液中是否含SO42- |
19.下列说法不正确的是( )
| A. | 氢能、太阳能、核能均为新能源 | |
| B. | 生物质能的利用主要有直接燃烧、生物化学转换和热化学转换等方式 | |
| C. | 通过煤的气化、液化等物理方法将煤转化为CO、CH4等燃料气体,可以提高煤燃烧的热效率 | |
| D. | 地球上最基本的能源是太阳能,大自然利用太阳能最成功的是植物的光合作用 |
6.某同学对无水乙醇与金属钠的反应进行实验探究.请回答:
(1)仪器a的名称是干燥管.
(2)请写出无水乙醇与钠反应的化学方程式:2CH3CH2OH+2Na=2CH3CH2ONa+H2.
(3)下列有关该实验的说法中,正确的是CD.
A.无水乙醇与钠的反应是吸热反应
B.酸性重铬酸钾溶液的作用是除去乙醇蒸气中混有的氢气
C.仪器a的球形区域对产生的气体起到一定的富集作用,使得气体燃烧的火焰明亮,现象明显
D.操作步骤②中的现象有:加入无水乙醇后,钠表面有气泡,钠开始时沉在液体的底部,然后浮在液面上,直至消失.
| 实验装置 | 操作步骤 | 实验现象 |
 | ①用橡胶管将尖嘴管和仪器a连接,向仪器a的球形区域塞入一团脱脂棉,再向脱脂棉中滴入适量的酸性K2Cr2O7溶液 | 棉花呈橙黄色 |
| ②取黄豆大小的金属钠,用滤纸吸干其表面的煤油,放入小烧杯中,用仪器a的柱体部分扣住金属钠,再向小烧杯中倒入10mL左右无水乙醇,至高度没过金属钠 | ||
| ③反应开始20s左右,点燃尖嘴管处的气体,并在尖嘴管上方罩上内壁涂有澄清石灰水的小烧杯 | 产生明亮的淡蓝色火焰,仪器a内的脱脂棉逐渐由橙黄色变为绿色(Cr3+颜色),烧杯内壁未变浑浊 | |
| ④实验结束后测量反应液的温度 | 反应液的温度为52℃ |
(2)请写出无水乙醇与钠反应的化学方程式:2CH3CH2OH+2Na=2CH3CH2ONa+H2.
(3)下列有关该实验的说法中,正确的是CD.
A.无水乙醇与钠的反应是吸热反应
B.酸性重铬酸钾溶液的作用是除去乙醇蒸气中混有的氢气
C.仪器a的球形区域对产生的气体起到一定的富集作用,使得气体燃烧的火焰明亮,现象明显
D.操作步骤②中的现象有:加入无水乙醇后,钠表面有气泡,钠开始时沉在液体的底部,然后浮在液面上,直至消失.
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 mL水中含有的分子数目约为1.24NA | |
| B. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 23g钠在氧气中完全燃烧失去电子数为0.5NA | |
| D. | 常温常压下的33.6L氯气与56g铁充分反应,转移电子数为3NA |
12.在强酸性无色溶液中,下列各组离子可能大量共存的是( )
| A. | Cu2+、NH4+、SO42-、Cl-、 | B. | Na+、K+、CO32-、Cl- | ||
| C. | K+、Fe2+、MnO4-、Cl- | D. | Na+、K+、NO3-、Cl- |