题目内容
5. 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.请回答下列问题:(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol.由上述方程式可知,CH3OH(g)的燃烧热大于(填“大于”、“等于”或小于”)192.9kJ/mol.已知水的气化热为44kJ/mol,则表示氢气燃烧热的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-124.6kJ/mol.
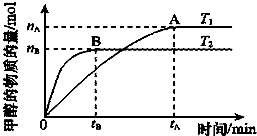
(2)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,温度对反应的影响,实验结果如图所示(注:T1、T2均大于300℃),该反应为放热反应(填“放热”或“吸热”);在T1温度时,将1mol CO2和3mol H2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为(2-a):2.
分析 (1)气态水的能量比较液态水的能量高;
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol.
水的气化热为44kJ/mol,可得:
③H2O(l)=H2O(g)△H=+44kJ/mol
根据盖斯定律,(②-①÷3)-③可得:H2(g)+$\frac{1}{2}$O2(g)=H2O(l);
(2)温度T2先达到平衡,则温度T2>T1,又温度高时平衡状态CH3OH的物质的量少,则说明升高温度,可逆反应CO2+3H2?CH3OH+H2O向逆反应方向移动;
CO2转化率为a,转化的二氧化碳为amol,则:
CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)
起始(mol):1 3 0 0
变化(mol):a 3a a a
平衡(mol):1-a 3-3a a a
相同条件下,气体的压强之比等于物质的量之比.
解答 解:(1)表示甲醇燃烧热,应是去mol甲醇燃烧生成二氧化碳与液态水,由于气态水的能量比较液态水的能量高,故生成液态水放出的热量更多,故CH3OH(g)的燃烧热大于192.9kJ/mol,
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(g)△H=-192.9kJ/mol.
水的气化热为44kJ/mol,可得:
③H2O(l)=H2O(g)△H=+44kJ/mol
根据盖斯定律,(②-①÷3)-③可得:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-124.6kJ/mol,
故答案为:大于;H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-124.6kJ/mol;
(2)温度T2先达到平衡,则温度T2>T1,又温度高时平衡状态CH3OH的物质的量少,则说明升高温度,可逆反应CO2+3H2?CH3OH+H2O向逆反应方向移动,故正反应为放热反应;
CO2转化率为a,转化的二氧化碳为amol,则:
CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)
起始(mol):1 3 0 0
变化(mol):a 3a a a
平衡(mol):1-a 3-3a a a
相同条件下,气体的压强之比等于物质的量之比,则容器内的压强与起始压强之比为=(1-a+3-3a+a+a):(1+3)=(2-a):2,
故答案为:放热;(2-a):2.
点评 本题主要考查了燃烧热、盖斯定律应用、化学平衡图象、化学平衡计算等,难度中等,注意对基础知识的理解掌握.

(1)测定目的:测定××牌软包装橙汁维生素C含量.
(2)测定原理:C6H8O6+I2→C6H6O6+2H++2I-.
(3)实验用品及试剂:
①仪器和用品(自选,略).
②试剂:指示剂淀粉(填名称)、浓度为7.50×10-3mol•L-1标准碘溶液、蒸馏水等.
(4)实验过程:
①洗涤仪器:检查滴定管是否漏液,润洗后装好标准碘溶液待用.
②打开橙汁包装,目测:颜色--橙黄色,澄清度--好.用酸式滴定管(或移液管)(填仪器名称)向锥形瓶中移入25.00mL待测橙汁,滴入2滴指示剂.
③用左手控制滴定管的活塞(填部位的名称),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化直到滴定终点.滴定至终点的现象是最后一滴标准液滴入,溶液由无色变为蓝色,且半分钟不褪色.
| 滴定次数 | 待测液体积/mL | 标准碘溶液体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均值 | ||
| 1 | 25.00 | 0.00 | 14.97 | ① |
| 2 | 25.00 | 0.10 | 15.13 | |
| 3 | 25.00 | 0.22 | 14.93 | |
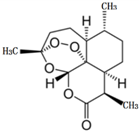 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )| A. | 青蒿素属于芳香化合物,能与H2发生加成反应 | |
| B. | 青蒿素能与氢氧化钠溶液发生反应 | |
| C. | 青蒿素的化学式为C15H22O5 | |
| D. | 青蒿素的核磁共振谱图中有12个峰 |
| A. | 0.6mol | B. | 1mol | C. | 1.3mol | D. | 0.8mol |
 减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
减少氮的氧化物在大气中的排放是环境保护的重要内容之一.(1)如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ•mol-1;
已知:N2(g)+2NO2(g)?4NO(g)△H=+292.3kJ•mol-1,
则反应:2NO(g)+2CO(g)?N2(g)+2CO2(g) 的△H=-760.3kJ•mol-1
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如下表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有D
A.升高温度 B.恒容充入氦气 C.恒容再充入NO2 D.把恒容改为恒压,其它条件相同.
| A. | 蛋白质溶液 | B. | 牛奶 | C. | 盐酸 | D. | 雾 |
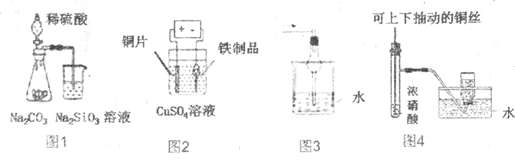
| A. | 图1为证明非金属性强弱:S>C>Si | |
| B. | 图2为在铁制品表面镀铜 | |
| C. | 图3可用于吸收氯化氢、溴化氢等气体 | |
| D. | 图4为制备并收集少量NO2气体 |




