题目内容
20.已知:①氯气(Cl2)是黄绿色气体,溴单质(Br2)是棕红色液体,碘单质(I2)是紫黑色固体,②氯化钠可以和浓硫酸反应生成硫酸钠和氯化氢.试根据下图所示的转化关系及实验现象,推断A一Y物质的化学式:
分析 由题给信息可知F为Br2,C和D反应生成Br2,C应为Cl2,D为KBr,E为KCl,KCl和浓硫酸生成A为HCl,黑色固体B为MnO2,X遇淀粉变蓝色,X为I2,则G应为KI,以此解答该题.
解答 解:由题给信息可知F为Br2,C和D反应生成Br2,C应为Cl2,D为KBr,E为KCl,KCl和浓硫酸生成A为HCl,黑色固体B为MnO2,X遇淀粉变蓝色,X为I2,则G应为KI,
故答案为:A:HCl;B:MnO2;C:Cl2;D:KBr;E:KCl;F:Br2.
点评 本题考查了无机物的推断,为高考常见题型,侧重于学生的分析能力和物质性质的应用,主要考查反应现象的判断应用,注意题给信息以及碘与淀粉的性质,难度不大.

练习册系列答案
相关题目
11.某气态烷烃和气态烯烃组成的混合气体,在相同条件下对氢气的相对密度为13;取该混合气体8.96L(标准状况)通入足量的溴水中,经充分吸收后,溴水的质量增加了5.6g,此混合气体的可能组成是( )
| A. | 甲烷和丙烯 | B. | 甲烷和丁烯 | C. | 乙烷和乙烯 | D. | 丙烷和乙烯 |
8.已知2H2O2(aq)=2H2O(l)+O2(g)△H=-196KJ•mol-1,常温下,往H2O2溶液中滴加少量FeCl2溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列有关反应的说法正确的是( )
| A. | 在H2O2分解过程中,溶液的pH逐渐下降 | |
| B. | Fe3+是该反应的催化剂 | |
| C. | 2H2O(l)+O2(g)=2H2O2(aq)在一定条件下能够自发进行 | |
| D. | v(H2O2)=2v(O2) |
15.下列离子或化学方程式与所述事实相符且正确的是( )
| A. | FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | |
| B. | 用K37ClO3与浓盐酸反应制氯气:K37ClO3+6HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$K37Cl+3Cl2+3H2O | |
| C. | 足量小苏打溶液与氢氧化钡溶液混合:Ba2++OH-+HCO3-═BaCO3↓+H2O | |
| D. | 向AlCl溶液中滴加过量的氨水:Al3++4OH-═[Al(OH)4]- |
2.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0.一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) | |
| C. | 保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,n(Z)=0.24 mol | |
| D. | 其他条件不变,向平衡体系中再充入0.16 mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大 |

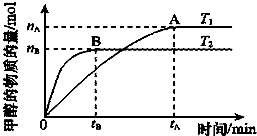 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.请回答下列问题:
 ,F中的含氧官能团名称酚羟基、羧基;
,F中的含氧官能团名称酚羟基、羧基; ;
; +2H2O.
+2H2O.