题目内容
11.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )| A. | 1 mol硫酸钾中阴离子所带电荷数为NA | |
| B. | 常温下,2.7克铝与足量的氢氧化钠溶液反应,失去的电子数为0.1NA | |
| C. | 在常温下,把100 g CaCO3加到1 L水中,所得溶液中的Ca2+数等于NA | |
| D. | 在标准状况下,22.4 L CH4与18 g H2O所含有的分子数均为NA |
分析 A.1mol硫酸钾中含有1mol硫酸根离子,带有2mol负电荷;
B.铝为+3价金属,2.7g铝的物质的量为0.1mol,反应后失去0.3mol电子;
C.碳酸钙为难溶物,溶液中钙离子的物质的量远远小于1mol;
D.标况下22.4L甲烷的物质的量为1mol,18g水的物质的量为1mol,二者含有的分子数相同.
解答 解:A.1 mol硫酸钾中含有1mol硫酸根离子,1mol硫酸根离子带有2mol负电荷,阴离子所带电荷数为2NA,故A错误;
B.2.7g铝的物质的量为0.1mol0.1mol铝与氢氧化钠溶液反应生成0.1mol偏铝酸钠,失去了0.3mol电子,失去的电子数为0.3NA,故B错误;
C.100g碳酸钙的物质的量为1mol,1mol碳酸钙加入1L水中,碳酸钙难溶于水,则溶液中的钙离子远远小于1mol,所得溶液中的Ca2+数远远小于NA,故C错误;
D.标况下22.4 L CH4的物质的量为:$\frac{22.4L}{22.4L/mol}$=0.1mol,18 g H2O的物质的量为:$\frac{18g}{18g/mol}$=1mol,所含有的分子数均为NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,C为易错点,注意碳酸钙为难溶物.

练习册系列答案
相关题目
2.下列各组物质可用分液漏斗分离的是( )
| A. | 乙酸与乙酸乙酯 | B. | 溴苯与水 | C. | 酒精与水 | D. | 苯与CCl4 |
19.下列离子方程式正确的是( )
| A. | 用CuSO4溶液将ZnS转化成CuS沉淀:S2-+Cu2+═CuS↓ | |
| B. | NH4HCO3溶液与过量NaOH溶液混合加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 向酸化的FeSO4溶液中滴入少量H2O2溶液:H2O2+2Fe2++2H+═2Fe3++2H2O | |
| D. | 用惰性电极电解饱和的KCl溶液:2H++2Cl$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2 |
6.某化合物通过化合反应生成,向其溶液中加入足量Na2O2,最终有白色沉淀产生.下列化合物中符合上述条件的是( )
| A. | Ca(HCO3)2 | B. | Na2SiO3 | C. | FeCl2 | D. | AlCl3 |
16.几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以和Z单质在放电条件下发生化合反应 |
3.化学在资源利用、环境保护等与社会可持续发展密切相关的领域发挥着积极作用.下列做法与社会可持续发展理念相违背的是( )
| A. | 改进汽车尾气净化技术,减少大气污染物的排放 | |
| B. | 开发利用可再生能源,减少化石燃料的使用 | |
| C. | 过度开采矿物资源,促进地方经济发展 | |
| D. | 研发可降解高分子材料,减少“白色污染” |
20.某元素的原子核外有三个电子层,其最外层电子数是次外层电子数的一半,则此元素是( )
| A. | Na | B. | Si | C. | P | D. | S |
1.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 6.2 g白磷(P4)中所含P-P键的数目为0.15NA(白磷分子结构 ) ) | |
| B. | 常温常压下,16 g 14CH4所含中子数为8NA | |
| C. | 117 g氯化钠固体中含有2NA个氯化钠分子 | |
| D. | 含5NA个电子的氨气中,氢原子数目为1.5NA |
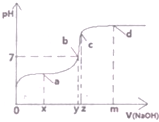 (1)25℃时,向20mL0.1mol•L的醋酸溶液中不断滴入0.1mol•L-1的NaOH溶液,溶液的pH变化曲线如图所示.
(1)25℃时,向20mL0.1mol•L的醋酸溶液中不断滴入0.1mol•L-1的NaOH溶液,溶液的pH变化曲线如图所示.