题目内容
中学化学中有很多物质可以实现下图中物质之间的转化.其中反应条件和部分反应的产物已略去.液体B和C可能是单一溶质的溶液,也可能是纯净物.

(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色.写出反应①的化学方程式 .
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈蓝色.写出反应①的离子方程式 ;
写出反应②的任意一个离子方程式 .
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液 (填“能”或“否”).

(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色.写出反应①的化学方程式
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈蓝色.写出反应①的离子方程式
写出反应②的任意一个离子方程式
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液
考点:无机物的推断
专题:推断题
分析:(1)根据气体D能使品红溶液褪色,加热时又恢复原色,可知D为SO2,由A是一种红色金属可知A为Cu,从而可知反应①为Cu和浓硫酸的反应;
(2)根据D是一种无色气体,遇到空气变为红棕色,应为NO,液体C呈蓝色,可推知反应①是铜与稀硝酸的反应;
(3)D是最轻的气体,应为H2,如B为NaOH溶液,则A为Al、C为NaAlO2,不能发生置换反应生成Al.
(2)根据D是一种无色气体,遇到空气变为红棕色,应为NO,液体C呈蓝色,可推知反应①是铜与稀硝酸的反应;
(3)D是最轻的气体,应为H2,如B为NaOH溶液,则A为Al、C为NaAlO2,不能发生置换反应生成Al.
解答:
解:(1)根据气体D能使品红溶液褪色,加热时又恢复原色,可知D为SO2,由A是一种红色金属可知A为Cu,从而可知反应①为Cu和浓硫酸的反应,反应的化学方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)D是一种无色气体,遇到空气变为红棕色,应为NO,液体C呈蓝色,说明A为Cu,B为稀硝酸,C为Cu(N03)2,反应①的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,反应②为置换反应,生成Cu,离子方程式可写为Cu2++Fe=Fe2++Cu等,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;Cu2++Fe=Fe2++Cu;
(3)D是最轻的气体,应为H2,如B为NaOH溶液,则A为Al、C为NaAlO2,不能发生置换反应生成Al,
故答案为:否.
| ||
故答案为:Cu+2H2SO4(浓)
| ||
(2)D是一种无色气体,遇到空气变为红棕色,应为NO,液体C呈蓝色,说明A为Cu,B为稀硝酸,C为Cu(N03)2,反应①的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,反应②为置换反应,生成Cu,离子方程式可写为Cu2++Fe=Fe2++Cu等,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;Cu2++Fe=Fe2++Cu;
(3)D是最轻的气体,应为H2,如B为NaOH溶液,则A为Al、C为NaAlO2,不能发生置换反应生成Al,
故答案为:否.
点评:本题考查无机物的推断,题目难度不大,把握物质的特征性质为推断的突破口,注意基础知识的掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法中用离子方程式表达正确的是( )


| A、用含氢氧化铝的药物治疗胃酸过多症:OH-+H+=H2O | ||||
B、用亚硫酸钾溶液吸收硫酸工业尾气中的SO2:SO2+S
| ||||
| C、右图所示电池的反应:Cu2++2Ag=Cu+2Ag+ | ||||
| D、用稀硫酸洗涤粘在试管壁上的氧化亚铜:Cu2O+2H+=2Cu2++H2O |
将质量相等的银片和铂片分别作为阳极和阴极用来电解硝酸银溶液
i.以电流强度为1A通电10分钟;
ii.10min后,反接电源,以电流强度为2A继续通电10分钟;下列图象分别表示:银电极质量,铂电极质量,及电解池产生气体质量和电解时间的关系图.正确的是( )

i.以电流强度为1A通电10分钟;
ii.10min后,反接电源,以电流强度为2A继续通电10分钟;下列图象分别表示:银电极质量,铂电极质量,及电解池产生气体质量和电解时间的关系图.正确的是( )

| A、①③ | B、①②③ |
| C、②③④ | D、①②③④ |
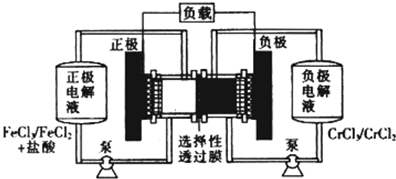
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+
Fe2++Cr3+.下列说法一定正确的是( )
| 放电 |
| 充电 |

| A、充电时,阴极的电极反应式为Cr3++e-=Cr2+ |
| B、电池放电肘,负极的电极反应式为Fe2+-e-=Fe3+ |
| C、电池放电时,Cl-从负极室穿过选择性透过膜移向正极室 |
| D、放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1mol.L-1 |


