题目内容
2.对于锂、钠、钾、铷、铯五种元素的单质或化合物的说法不正确的是( )| A. | 随着电子层数的增加单质的密度逐渐升高 | |
| B. | 随着核电荷数的增加单质的熔点逐渐降低 | |
| C. | 在自然界中都只能以化合态形式存在 | |
| D. | 单质都能与水反应,且反应后的溶液都呈碱性 |
分析 依据同主族元素性质递变规律解答:碱金属元素从上到下密度依次增大(钠、钾反常),熔沸点依次降低,金属性依次增强,据此解答;
解答 解:锂、钠、钾、铷、铯都是碱金属元素,在周期表中位置从上到下排列为:锂、钠、钾、铷、铯,
A.碱金属元素从上到下密度依次增大(钠、钾反常),故A错误;
B.碱金属元素从上到下随着核电荷数的增加单质的熔点逐渐降低,故B正确;
C.锂、钠、钾、铷、铯性质活泼容易与空气中的水、氧气反应,所以自然界中只能以化合态存在,故C正确;
D.锂、钠、钾、铷、铯性质活泼都能与水反应依次生成氢氧化锂、氢氧化钠、氢氧化钾、氢氧化铯,同时都生成氢气,故D正确;
故选:A.
点评 本题考查了碱金属元素的性质,明确同主族元素性质的递变规律是解题关键,题目难度不大,注意钠的密度大于钾.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
13.下列体系加压后,对化学反应速率没有影响的是( )
| A. | 2SO2+O2?2SO3 | B. | CO2+H2O?H2CO3 | C. | CO+H2O(g)?CO2+H2 | D. | H++OH-?H2O |
10.以下电子排布式表示基态原子电子排布的是( )
| A. | 1s22s22p63s13p3 | B. | 1s22s22p63s23p63d104s14p1 | ||
| C. | 1s22s22p63s23p63d24s2 | D. | 1s22s22p63s23p63d104s14p2 |
17.下列各有机物的名称错误的是( )
| A. | 3-甲基-2-戊烯 | B. | 2,2-二甲基丙烷 | C. | 3-甲基-1-丁烯 | D. | 3-甲基-2-丁烯 |
7.C、CO、CH4、C2H5OH是常用的燃料,它们每1g分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为32.8kJ、10.1kJ、55.6kJ、29.7kJ.相同物质的量的这四种燃料,完全燃烧时放出热量最少的是( )
| A. | C | B. | CO | C. | CH4 | D. | C2H5OH |
14.化学实验操作中必须十分重视安全问题.下列处理方法不正确的是( )
| A. | 不慎打翻燃着的酒精灯,立即用湿抹布盖灭 | |
| B. | 浓碱液滴在皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 给盛有液体的试管加热时,要不断移动试管或加入碎瓷片 | |
| D. | 金属钠着火时,立即用泡沫灭火器进行灭火 |
11.如图是部分短周期主族元素原子半径与原子序数的关系图.下列说法错误的是( )
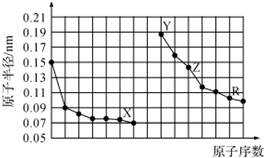

| A. | X、Y分别是O、Na元素 | |
| B. | R的单质与足量X2反应生成RX3 | |
| C. | Z的氧化物熔点很高,是较好的耐火材料 | |
| D. | 电解熔融的Z的氧化物可以得到单质Z |