题目内容
 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.(1)写出该反应的反应方程式:
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是
(4)试管中收集气体是
考点:性质实验方案的设计,实验装置综合
专题:实验设计题
分析:(1)Fe与水蒸气高温反应生成四氧化三铁和氢气,Fe元素的化合价升高,H元素的化合价降低;
(2)装置受热后,水转化为水蒸气,烧瓶底部放置了几片碎瓷片,可防止液体剧烈沸腾;
(3)如果在一套装置中需要两处加热,一定要注意点燃加热仪器的顺序,一般是根据实验的安全性和对实验结果的影响来考虑;
(4)点燃氢气前一定要检验纯度,防止发生爆炸.
(2)装置受热后,水转化为水蒸气,烧瓶底部放置了几片碎瓷片,可防止液体剧烈沸腾;
(3)如果在一套装置中需要两处加热,一定要注意点燃加热仪器的顺序,一般是根据实验的安全性和对实验结果的影响来考虑;
(4)点燃氢气前一定要检验纯度,防止发生爆炸.
解答:
解:(1)Fe与水蒸气高温反应生成四氧化三铁和氢气,反应为3Fe+4H2O(g)
Fe3O4+4H2,Fe元素的化合价升高,H元素的化合价降低,则Fe为还原剂,水为氧化剂,故答案为:3Fe+4H2O(g)
Fe3O4+4H2;Fe;水;
(2)装置受热后,水转化为水蒸气,则作用为为实验提供水蒸气;烧瓶底部放置了几片碎瓷片,可防止液体剧烈沸腾,则作用为防止暴沸,故答案为:为实验提供水蒸气;防止暴沸;
(3)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,排掉硬质玻璃管内空气,为Fe与水蒸气的反应实验提供持续不断的水蒸气,
故答案为:先点燃酒精灯,后点燃酒精喷灯;
(4)由发生的反应及干燥可知,最后只收集到H2,氢气的爆炸极限是4.0%~75.6%,氢气不纯加热易引起爆炸,因此,点燃之前要检验纯度,
故答案为:H2;检验纯度.
| ||
| ||
(2)装置受热后,水转化为水蒸气,则作用为为实验提供水蒸气;烧瓶底部放置了几片碎瓷片,可防止液体剧烈沸腾,则作用为防止暴沸,故答案为:为实验提供水蒸气;防止暴沸;
(3)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,排掉硬质玻璃管内空气,为Fe与水蒸气的反应实验提供持续不断的水蒸气,
故答案为:先点燃酒精灯,后点燃酒精喷灯;
(4)由发生的反应及干燥可知,最后只收集到H2,氢气的爆炸极限是4.0%~75.6%,氢气不纯加热易引起爆炸,因此,点燃之前要检验纯度,
故答案为:H2;检验纯度.
点评:本题考查性质实验方案的设计,为高频考点,把握发生的反应及实验装置的作用为解答的关键,侧重分析及实验能力的考查,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
断肠草(Gelsemium)为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构简式,下列推断正确的是( )


| A、②中所含官能团种类比③中多 |
| B、①、④互为同系物 |
| C、①、②、③、④均能与氢氧化钠溶液反应 |
| D、等物质的量②、③分别在足量氧气中完全燃烧,前者消耗氧气比后者少 |
下列物质中,既能与盐酸反应,又能跟NaOH溶液反应的是( )
①NaHCO3②Al ③Al2O3④Al(OH)3⑤NaAlO2.
①NaHCO3②Al ③Al2O3④Al(OH)3⑤NaAlO2.
| A、全部 | B、②③⑤ |
| C、①③⑤ | D、①②③④ |
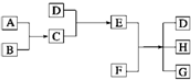 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示:

 为原料合成重要的化工产品
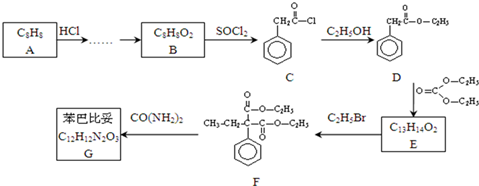
为原料合成重要的化工产品 .合成路线流程图示例如下:
.合成路线流程图示例如下: .
.



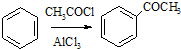 ,请设计合理方案以B的同系物
,请设计合理方案以B的同系物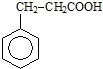 为原料合成
为原料合成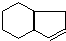 (用合成路线流程图表示为:A
(用合成路线流程图表示为:A
