题目内容
已知难溶于水的盐在水中存在溶解平衡:AgCl(s)
Ag++Cl-在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,称为沉淀溶解平衡常数,可用 Ksp表示:Ksp=c(Ag+)?c(Cl-?)=1.8×10?-10.
(1)向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀,说明氯化银的溶解度 碘化银的溶解度(填“大于”、“小于”或“等于”),由此得出的结论是
(2)在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp (填“增大”、“减小”或“不变”).
(3)若把足量AgCl分别放入①100mL0.1mol/L稀硝酸,②100mL 0.1mol/L NaCl溶液,③100mL 0.1mol/L AlCl3溶液,④100mL 0.1mol/L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 .在0.1mol/L AlCl3溶液中,Ag+的物质的量浓度最多为 mol/L.
| 溶解 |
| 沉淀 |
(1)向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀,说明氯化银的溶解度
(2)在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp
(3)若把足量AgCl分别放入①100mL0.1mol/L稀硝酸,②100mL 0.1mol/L NaCl溶液,③100mL 0.1mol/L AlCl3溶液,④100mL 0.1mol/L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:(1)根据难溶电解质的沉淀转化判断;
(2)溶度积只受温度的影响;
(3)依据在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP=c(Ag+)?c(Cl-)=1.8×10-10;温度不变,Ksp不变,分别计算银离子浓度比较.
(2)溶度积只受温度的影响;
(3)依据在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP=c(Ag+)?c(Cl-)=1.8×10-10;温度不变,Ksp不变,分别计算银离子浓度比较.
解答:
解:(1)向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀,说明氯化银的溶解度大于碘化银的溶解度,由此可得出溶解度小的沉淀可转化成溶解度更小的沉淀,
故答案为:大于;溶解度小的沉淀可转化成溶解度更小的沉淀;
(2)溶度积只受温度的影响,温度不变,则溶度积不变,故答案为:不变;
(3)Ksp=1.8×10-10mol2?L-2=C(Ag+)?C(Cl-),通过计算分别得到:
①100mL蒸馏水中含银离子浓度和氯离子浓度相同;
②100mL 0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;
③1000mL 0.1mol?L-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;
④100mL 0.01mol?L-1MgCl2溶液中Cl-浓度为0.02mol/l,抑制沉淀溶解平衡,银离子浓度=
=9×10-9mol/L;
综上所述大小顺序为:①④②③;③在0.1mol?L-1氯化铝溶液中,银离子的物质的量浓度最大可达到:6.0×10-10mol/L.
故答案为:①>④>②>③;6×10 -10.
故答案为:大于;溶解度小的沉淀可转化成溶解度更小的沉淀;
(2)溶度积只受温度的影响,温度不变,则溶度积不变,故答案为:不变;
(3)Ksp=1.8×10-10mol2?L-2=C(Ag+)?C(Cl-),通过计算分别得到:
①100mL蒸馏水中含银离子浓度和氯离子浓度相同;
②100mL 0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;
③1000mL 0.1mol?L-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;
④100mL 0.01mol?L-1MgCl2溶液中Cl-浓度为0.02mol/l,抑制沉淀溶解平衡,银离子浓度=
| 1.8×10-10 |
| 0.02 |
综上所述大小顺序为:①④②③;③在0.1mol?L-1氯化铝溶液中,银离子的物质的量浓度最大可达到:6.0×10-10mol/L.
故答案为:①>④>②>③;6×10 -10.
点评:本题考查了难溶物质的沉淀溶解平衡的应用,溶度积的计算应用,为高频考点,侧重学生的分析、计算能力的考查,注意溶度积是随温度变化,不随浓度变化,题目难度中等.

练习册系列答案
相关题目
下列有关实验的做法或说法正确的是( )
| A、在制备乙烯的实验中,为了防止反应产生副产物,加热时应使温度迅速上升至170°C |
| B、分别向三支盛有乙酸乙酯的试管中加入氢氧化钠溶液、稀硫酸、水,并在水浴中加热,乙酸乙酯香味散失的速度按氢氧化钠、水、稀硫酸的顺序依次减慢 |
| C、将溴乙烷滴入NaOH溶液中,待充分反应再加入AgNO3溶液后有浅黄色沉淀生成 |
| D、向苯酚钠稀溶液中,通入少量二氧化碳气体,溶液中生成碳酸钠 |
丙烯醇(CH2═CH-CH2OH)可发生的化学反应有( )
①加成 ②氧化 ③燃烧 ④与钠反应.
①加成 ②氧化 ③燃烧 ④与钠反应.
| A、①②③ | B、②③④ |
| C、①②③④ | D、①③④ |
关于Fe(OH)2 的制备能够成功的是( )
| A、向FeCl2 溶液中逐滴加入NaOH溶液 |
| B、向FeSO4溶液中逐滴加入氨水 |
| C、先将盛有NaOH溶液的长滴管插到FeSO4液面下,再挤出NaOH溶液可制得Fe(OH)2的白色沉淀 |
| D、取新配制的FeSO4溶液适量放入试管中,在加入一层植物油(密度小于水,且不溶于水),然后向试管内逐滴加入NaOH溶液 |
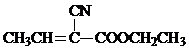 )是合成某种手术用粘合剂的单体,X的合成路线如图:
)是合成某种手术用粘合剂的单体,X的合成路线如图: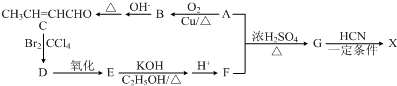


 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.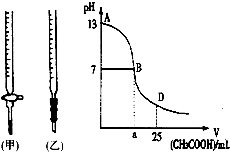 图为向25mL0.1mol?L-1NaOH溶液中逐渐滴加0.2mol?L-1CH3COOH溶液过程中,用pH计跟踪测出溶液pH的变化曲线,请回答:
图为向25mL0.1mol?L-1NaOH溶液中逐渐滴加0.2mol?L-1CH3COOH溶液过程中,用pH计跟踪测出溶液pH的变化曲线,请回答: