题目内容
8.实验室用硫酸铝酸性溶液制备可溶性的碱式硫酸铝[Ala(SO4)b(OH)c],并用它对烟气进行脱硫处理的过程如图1: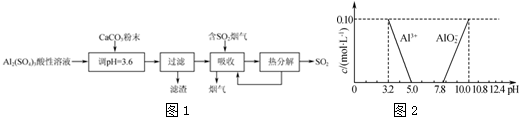
(1)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Ala(SO4)b(OH)c.过滤时所用的玻璃仪器有漏斗、玻璃棒和烧杯,滤渣的主要成分为CaSO4(填化学式).
(2)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是溶液中的部分SO32- 被氧化成SO42-;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将减小(填“增大”“减小”或“不变”).
(3)Ala(SO4)b(OH)c中a、b、c的代数关系式为3a=2b+c.
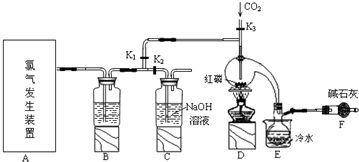
(4)已知在常温下溶液中Al3+、AlO2-的浓度与溶液pH的关系如图2所示.为确定碱式硫酸铝的组成,进行如下实验:
①取2.18g碱式硫酸铝样品在空气中灼烧至恒重,样品质量减少了0.36g.
②另取2.18g碱式硫酸铝溶于水,调节溶液的pH到5.0~7.8.
③将②产生的沉淀过滤、洗涤、灼烧至恒重,称量剩余固体为1.02g.
请计算样品中Al3+和SO42-的物质的量之比(写出计算过程).
分析 根据流程可知,Al2(SO4)3溶液中加入CaCO3调节溶液的pH至3.6,使Al2(SO4)3转化为CaSO4沉淀,过滤得滤渣为CaSO4,滤液中含有铝离子、硫酸根离子等,吸收含有二氧化硫的烟气,在溶液中生成亚硫酸根离子,部分亚硫根离子会被空气氧化成硫酸,将溶液再加热亚硫酸盐分解生成二氧化硫,所得溶液循环利用再用来吸收烟气,
(1)过滤时所用的玻璃仪器有漏斗、玻璃棒、烧杯;硫酸根离子与钙离子反应生成硫酸钙是微溶于水的物质,易形成沉淀;
(2)在溶液中SO32-易被氧化生成SO42-,弱酸根离子转化为强酸根离子溶液酸性增强;
(3)根据化合物中化合价代数和为零可知abc的关系;
(4)碱式硫酸铝样品在空气中灼烧至恒重,样品中的氢元素全部以水的形式失去,根据水的质量可求得样品中氢氧根离子的物质的量,在硫酸铝溶液中,随着pH值的升高,调节溶液的pH到5.0~7.8,生成氢氧化铝沉淀,氢氧化铝沉淀经过过滤、洗涤、灼烧至恒重,得氧化铝,根据氧化铝的质量可求得样品中铝元素的物质的量,根据电荷守恒可求得硫酸根离子的物质的量,据此确定品中Al3+和SO42-的物质的量之比.
解答 解:根据流程可知,Al2(SO4)3溶液中加入CaCO3调节溶液的pH至3.6,使Al2(SO4)3转化为CaSO4沉淀,过滤得滤渣为CaSO4,滤液中含有铝离子、硫酸根离子等,吸收含有二氧化硫的烟气,在溶液中生成亚硫酸根离子,部分亚硫根离子会被空气氧化成硫酸,将溶液再加热亚硫酸盐分解生成二氧化硫,所得溶液循环利用再用来吸收烟气,
(1)过滤时所用的玻璃仪器有漏斗、玻璃棒、烧杯,通过以上分析知,滤渣的成分是CaSO4,
故答案为:漏斗、玻璃棒;CaSO4;
(2)溶液吸收二氧化硫生成SO32-,在溶液中SO32-易被氧化生成SO42-,所以上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量;溶液中SO32-属于弱酸根离子被氧气氧化为转化为SO42-,SO42-为强酸根离子,则溶液酸性增强,pH减小;
故答案为:溶液中的部分SO32- 被氧化成SO42-;减小;
(3)根据化合物中化合价代数和为零可知abc的关系为3a=2b+c,
故答案为:3a=2b+c;
(4)由步骤①可知n(H2O)=0.36 g/18 g•mol-1=0.02 mol,所以n(OH-)=0.02 mol×2=0.04 mol,
由③可知1.02 g为Al2O3,则n(Al2O3)=1.02 g/102 g•mol-1=0.01 mol,所以样品中n(Al3+)=0.02 mol 根据电荷守恒可知,样品中n(SO42-)=(0.02 mol×3-0.04 mol)/2=0.01 mol,所以n(Al3+):n(SO42-)=0.02 mol:0.01mol=2:1,
答:样品中Al3+和SO42-的物质的量之比为2:1.
点评 本题考查了物质的制备原理及化学计算,明确物质的性质及各物质的关系是解本题关键,会从整体上分析每一步发生的反应及基本操作,知道加入物质的用途,题目难度中等.

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
| A. | X难溶于乙醇 | |
| B. | 酒中的少量丁酸能抑制X的水解 | |
| C. | 分子式为C4H8O2且官能团与X相同的物质共有5种 | |
| D. | X完全燃烧后生成CO2和H20的物质的量比为1:2. |
 常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知Ksp(CaSO4)=9×10-6.下列说法不正确的是( )
常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知Ksp(CaSO4)=9×10-6.下列说法不正确的是( )| A. | a点对应的Ksp等于c点对应的Ksp | B. | 加入Na2SO4溶液可以使a点变为b点 | ||
| C. | a点变为b点将有沉淀生成 | D. | d点未达到沉淀溶解平衡状态 |
已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇O2会生成POCl3(三氯氧磷),POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl.PCl3、POCl3的熔沸点见下表.
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)写出A中反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B装置中所盛试剂是浓硫酸;E中烧杯内冷水的作用是冷凝PCl3防止其挥发便于收集产品.
(3)检查装置气密性后,向D装置的曲颈瓶中加入红磷,打开K3通入干燥的CO2,一段时间后关闭K3,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行.其中通入干燥CO2的目的是排尽曲颈瓶中的空气,防止PCl3与O2等发生副反应.
(4)实验制得的粗产品中常含有POCl3、PCl5等,加入红磷加热除去PCl5后,再通过蒸馏(填实验名称)即可得到较纯净的PCl3.
(5)实验后关闭K1,打开K2,将A、B中剩余氯气通入300ml 1mol/L的NaOH溶液中.若NaOH恰好完全反应,(假设反应生成了NaCl、NaClO 和 NaClO3 等钠盐),则反应中转移电子的物质的量(n)的范围是0.15mol<n<0.25mol.
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 加入NaHCO3使氯水的漂白能力增强 | |
| C. | 难溶电解质可以由溶解度小的转化为溶解度更小的,但不能从溶解度小的转化为溶解度大的 | |
| D. | Ksp只受温度的影响,不受浓度的影响 |
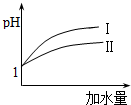 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+△H>0.
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+△H>0.
 CH3COOCH2CH3+H2O,酯化反应或取代反应.
CH3COOCH2CH3+H2O,酯化反应或取代反应.