题目内容
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且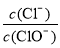 的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
A.若某温度下,反应后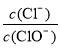 =11,则溶液中
=11,则溶液中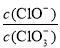 =
=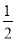
B.参加反应的氯气的物质的量等于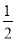 a mol
a mol
C.改变温度,产物中KClO3的最大理论产量为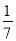 mol
mol
D.改变温度,反应中转移电子的物质的量ne的范围: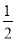 a mol≤ne≤
a mol≤ne≤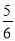 a mol
a mol
C
【解析】
试题分析:A.若某温度下,反应后 =11,则根据氧化还原反应中电子守恒可得1×c(Cl-)= 1×c(ClO-)+ 5×c(ClO3-), c(ClO3-)=2,则溶液中
=11,则根据氧化还原反应中电子守恒可得1×c(Cl-)= 1×c(ClO-)+ 5×c(ClO3-), c(ClO3-)=2,则溶液中 =
= ,正确;B.在反应后的产物中Cl元素与K元素的原子个数比为1:1,因为n(KOH)=a mol所以参加反应的氯气的物质的量等于
,正确;B.在反应后的产物中Cl元素与K元素的原子个数比为1:1,因为n(KOH)=a mol所以参加反应的氯气的物质的量等于 a mol,正确;C.改变温度,若产物中被氧化的Cl完全变为KClO3,根据元素守恒和电子守恒可知KClO3的最大理论产量为
a mol,正确;C.改变温度,若产物中被氧化的Cl完全变为KClO3,根据元素守恒和电子守恒可知KClO3的最大理论产量为 mol,错误;D.改变温度,若氧化产物完全变为KClO,则反应中转移电子的物质的量ne=
mol,错误;D.改变温度,若氧化产物完全变为KClO,则反应中转移电子的物质的量ne= a mol;若完全氧化KClO3,则反应中转移电子的物质的量ne=
a mol;若完全氧化KClO3,则反应中转移电子的物质的量ne= a mol,所以反应中转移电子的物质的量的范围:
a mol,所以反应中转移电子的物质的量的范围: a mol≤ne≤
a mol≤ne≤ a mol,正确。
a mol,正确。
考点:考查守恒方法在有关氧化还原反应的计算的应用的知识。

练习册系列答案
相关题目




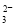 ===HCO
===HCO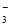 ③CO2+H2O+ClO-===HClO+HCO
③CO2+H2O+ClO-===HClO+HCO