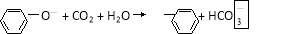题目内容
在200 mL某硫酸盐溶液中含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为( )
A.1 mol/L B.2 mol/L C.2.5 mol/L D.5 mol/L
C
【解析】
试题分析:n(SO42-)=1.5mol;n(金属阳离子)=1mol, n(金属阳离子)::n(SO42-)=2:3,在物质化学式中电荷守恒,所以物质的化学式是M2(SO4)3;n(M2(SO4)3)=0. 5 mol;该物质的浓度是c(M2(SO4)3)= 0. 5 mol÷0.2L=2.5 mol/L .故选项是C。
考点:考查电解质电离产生的离子、电解质的化学式的关系及物质的物质的量浓度的计算的知识。

练习册系列答案
相关题目
下列根据实验操作和现象所得出的结论正确的是
| 实验操作 | 实验现象 | 结论 |
A | 淀粉与稀H2SO4共热,再加银 氨溶液水浴加热 | 无银镜生成 | 淀粉水解产物无还原性 |
B | 向某溶液中先滴加氯水,再滴 加少量KSCN溶液 | 溶液变成血红色 | 溶液中含有Fe2+ |
C | 向NaAlO2溶液中滴加饱和 NaHCO3溶液 |
有白色沉淀产生 | 验证两者都发生了水解反 应,且相互促进 |
D | 将CO2通入Na2SiO3溶液中 | 有白色沉淀生成 | 证明H2CO3酸性比H2SiO3强 |
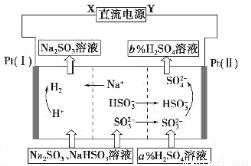
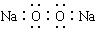 B.二氧化硅的分子式SiO2
B.二氧化硅的分子式SiO2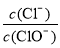 的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )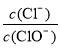 =11,则溶液中
=11,则溶液中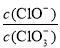 =
=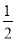
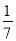 mol
mol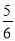 a mol
a mol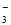 ===CaCO3↓+H2O
===CaCO3↓+H2O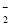 +4NH
+4NH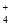 +2H2O
+2H2O
 + Ca2+ + OH- = CaCO3↓ + H2O
+ Ca2+ + OH- = CaCO3↓ + H2O = Fe3++ NO↑ + 2H2O
= Fe3++ NO↑ + 2H2O