题目内容
3.红矾钠(重铬酸钠:Na2Cr2O7•2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛.(1)实验室中红矾钠可用铬铁矿(主要成分:FeO•Cr2O3)利用以下过程来制取.

①步骤I中反应的化学方程式为:
4FeO•Cr2O3(s)+8Na2CO3(s)+7O2=8Na2Cro4(s)+2Fe2O3+8CO2该反应的化学平衡常数的表达式为K=$\frac{c(C{O}_{2})^{8}}{c({O}_{2})^{7}}$,在常温下该反应速度极慢,下列措施中能使反应速率增大的是ABC.
A.升高温度 B.通入过量的空气 C.将原料粉碎 D.增加纯碱的用量
②步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是NaA1O2[或NaA1(OH)4]、Na2SiO3.
③步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是除去A1O-2、SiO32-等杂质.
④步骤Ⅳ中发生反应的离子方程式为:2CrO42-+2H+=Cr2O72-+H2O.
(2)将红矾钠与KCl固体按1:2(物质的量比)混合溶于水后经适当操作可得到K2Cr2O7晶体.请填写表中空格,完成上述过程.(已知:在室温下重铬酸钾溶解度很小,而在升高温度时,其溶解度大大增加).
| 序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
| ① | 溶解 | 将混合物放入烧杯中,加入热的蒸馏水,充分搅拌直到固体不再溶解. |
| ② | ||
| ③ | ||
| ④ | ||
| ⑤ | 过滤、干燥 | 得到K2Cr2O7晶体 |
分析 (1)①根据平衡常数的表达式及书写要求写出该反应的平衡常数;根据影响化学反应速率的因素进行判断;
②铝、硅的氧化物在碱性条件下能够与氢氧根离子反应生成偏铝酸钠、硅酸钠;
③步骤Ⅱ中铝元素、硅元素以偏铝酸根离子、硅酸根离子形式存在,通过条件pH后可以将硅酸根离子、偏铝酸根离子转化成沉淀而除去;
④步骤Ⅳ中CrO42-在酸性条件下转化成Cr2O72-,据此写出反应的离子方程式;
(2)根据温度对各物质的溶解度大小进行分析.
解答 解:(1)①反应4FeO•Cr2O3(s)+8Na2CO3(s)+7O2=8Na2CrO4(s)+2Fe2O3+8CO2中,FeO•Cr2O3、Na2CO3、Na2CrO4、Fe2O3为固体,在平衡常数表达式中不需要出现,则该反应的平衡常数表达式为:K=$\frac{c(C{O}_{2})^{8}}{c({O}_{2})^{7}}$;
A.升高温度,可以加快反应速率,故A正确;
B.通入过量的空气,增大了氧气的量,可以加快反应速率,故B正确;
C.将原料粉碎,增大了接触面积,可以加快反应速率,故C正确;
D.纯碱是固体,不涉及浓度问题,所以改变纯碱的量,不能改变反应速率,故D错误;
故答案为:K=$\frac{c(C{O}_{2})^{8}}{c({O}_{2})^{7}}$;ABC;
②氧化铝、二氧化硅能够与氢氧根离子反应生成偏铝酸钠、硅酸钠,则碱性条件下,铝元素与硅元素的存在形式为NaAlO2、Na2SiO3,
故答案为:NaA1O2[或NaA1(OH)4];Na2SiO3;
③步骤Ⅲ需将溶液的pH调至7~8并煮沸,NaAlO2、Na2SiO3等杂质可以以沉淀的形式除去,
故答案为:除去A1O-2、SiO32-等杂质;
④该步骤是CrO42-到Cr2O72-的转化,反应的离子方程式为:2CrO42-+2H+=Cr2O72-+H2O,
故答案为:2CrO42-+2H+=Cr2O72-+H2O;
(2)根据Na2Cr2O7+2KCl=K2Cr2O7+2NaCl,向Na2Cr2O7中加入KCl固体,加热时重铬酸钾溶解度随着温度的升高而增大,但氯化钾的溶解度受温度的影响不大,则获得K2Cr2O7的操作方法分别为:溶解、蒸发、过滤、冷却、结晶、过滤、干燥,
故答案为:
| ② | 蒸发 | 将所得溶液转移至蒸发皿中,加热蒸发溶液使NaC1结晶析出 |
| ③ | 过滤 | 趁热过滤,将NaC1晶体与溶液分离 |
| ④ | 冷却,结晶 | 冷却滤液使K2Cr2O7结晶析出 |
点评 本题考查了制备方案的设计,题目难度中等,明确实验目的为解答关键,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力,注意掌握物质制备方案的设计原则.

| A. | 无色溶液中:Al3+、Cl-、MnO4-、SO42- | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、SCN- | |
| C. | 0.1 mol•L-1AgNO3溶液:H+、K+、SO42-、I- | |
| D. | 使酚酞变红色的溶液:CO32-、Cl-、F-、K+ |
| A. | 少量CO2通入过量氨水中:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 含等物质的量的NH4HSO3与NaOH溶液混合加热:HSO3-+OH-$\frac{\underline{\;△\;}}{\;}$SO32-+H2O | |
| C. | 溴化亚铁溶液中通入少量Cl2:Cl2+2Br-═2Cl-+Br2 | |
| D. | 含1molKOH的溶液与含2molBa(HCO3)2的溶液混合:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O |
| A. | 试用分液漏斗分液时,应将漏斗颈上的玻璃塞打开 | |
| B. | 蒸馏实验不一定使用温度计 | |
| C. | 用CCl4萃取碘水中的碘 | |
| D. |  过滤(如图)时,可将悬浊液从烧杯直接倒入漏斗中 过滤(如图)时,可将悬浊液从烧杯直接倒入漏斗中 |
| A. | 沸腾炉 | B. | 接触室 | C. | 高炉 | D. | 吸收塔 |
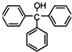 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇其合成流程如图1所示,装置如图2所示.
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇其合成流程如图1所示,装置如图2所示.已知:(I)格氏试剂容易水解,
 ;
;
(Ⅱ)相关物质的物理性质如下:
| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、笨等有机溶剂 |
| 溴苯 | -30.7℃ | 156.2℃ | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸已酯 | -34.6℃ | 212.6℃ | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,不溶于醇、醚等有机溶剂 | |
(1)图2中玻璃仪器B的名称:冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解;
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;制取格氏试剂时要保持微沸,可以采用水浴(方式)加热,优点是受热均匀,温度易于控制;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下 提纯方案,请填写如下空白:
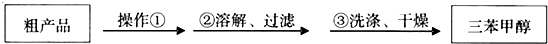
其中,①操作为蒸馏;洗涤液最好选用:A(从选项中选);A、水 B、乙醚 C、乙醇 D、苯
检验产品已经洗涤干净的操作为:取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已洗涤干净,反之则未洗涤干净
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80m L(标准状况).产品中三苯甲醇质量分数为90%(保留两位有效数字.
| A. | MgBr2 | B. | Na2S | C. | KI | D. | KCl |

 某研究性学习小组参照课文中的实验装置图做高温下铁与水蒸气反应的实验装置如图.在玻璃管中放入铁粉和石棉绒的混合物,加热,并通入水蒸气.用试管收集产生的干燥气体,并靠近火焰点火,观察现象.请回答下列问题:
某研究性学习小组参照课文中的实验装置图做高温下铁与水蒸气反应的实验装置如图.在玻璃管中放入铁粉和石棉绒的混合物,加热,并通入水蒸气.用试管收集产生的干燥气体,并靠近火焰点火,观察现象.请回答下列问题: