题目内容
17.硫的化合物在工业上有广泛的应用,因此研究硫的化合物制备有着重要的意义.某同学拟采用下图装置(实验前已除尽装置内的空气)来制取焦亚硫酸钠(Na2S2O5).已知装置图1Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2═Na2S2O3(1)装置I是用亚硫酸钠固体和浓硫酸制备二氧化硫气体,该装置中反应的化学方程式为Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O.如果想控制反应速度,图2中可选用的发生装置是ac(填写字母).

(2)装置Ⅱ中有Na2S2O5晶体析出,要获得已析出的晶体可采取的分离方法是过滤;
(3)装置Ⅲ用于处理尾气,可选用的最佳试剂是b(填序号).
a、饱和食盐水 b、NaOH溶液 c、浓硫酸 d、饱和NaHCO3溶液
(4)Na2S2O5与稀硫酸反应放出SO2,其离子方程式为S2O52-+2H+=2SO2↑+H2O
(5)工业制备得到产品Na2S2O5中含有杂质碳酸钠检验产品中含有碳酸钠杂质所需试剂是①③⑥或①②③⑥(填 编号)(已知Na2S2O5溶于水即生成NaHSO3)
①酸性高锰酸钾②品红溶液③澄清石灰水④饱和碳酸氢钠溶液⑤NaOH⑥稀硫酸
(6)葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中坑氧化剂的残留量(以游离SO2计算)的方案如下
葡萄酒样品20.00mL$→_{蒸馏}^{盐酸}$馏分$→_{用0.0105mol/L的标准I_{2}溶液滴}^{一定条件,淀粉溶液}$溶液出现蓝色且30s内不褪色
(已知:滴定时反映的化学方程式为SO2+I2+2H2O═H2SO4+2HI)
按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中坑氧化剂的残留量(以游离SO2计算)为0.84g.L-1.
分析 (1)装置Ⅰ中产生的气体为SO2,亚硫酸钠与硫酸反应生成硫酸钠、二氧化硫与水;根据分液漏斗和长颈漏斗的特点结合气压原理来回答;
(2)固体和液体的分离采用过滤法;
(3)二氧化硫属于酸性氧化物,有毒,要处理尾气,容易和氢氧化钠反应生成盐和水;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水;
(5)检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液,并用品红(或酸性高锰酸钾)检验是否除净,或直接用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净;
(6)由消耗碘的量,结合SO2+I2+2H2O═H2SO4+2HI计算二氧化硫的质量,进而计算浓度.
解答 解:(1)装置Ⅰ中亚硫酸钠与硫酸反应生成硫酸钠、二氧化硫与水,反应方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,如果想控制反应速度,用分液漏斗比长颈漏斗好得多,a装置可以,保证气压畅通,液体顺利留下,如图2中还可选用的发生装置是c,
故答案为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;ac;
(2)装置Ⅱ中有Na2S2O5晶体析出,固体和液体的分离采用过滤法,所以要获得已析出的晶体可采取的分离方法是过滤,
故答案为:过滤;
(3)二氧化硫有毒,要处理尾气,属于酸性氧化物,更容易和强碱氢氧化钠反应,饱和食盐水和二氧化硫不反应,浓硫酸不吸收二氧化硫,饱和NaHCO溶液和二氧化硫反应生成二氧化碳,不及氢氧化钠吸收效果好,所以最佳试剂应该选择b,
故答案为:b;
(4)Na2S2O5与稀硫酸反应生成SO2,反应中S元素的化合价未发生变化,同时生成硫酸钠与水,反应离子方程式为:S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O;
(5)检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液,并用品红(或酸性高锰酸钾)检验是否除净,或直接用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,检验产品中含有碳酸钠杂质所需试剂是①③⑥或①②③⑥,
故答案为:①③⑥或①②③⑥;
(6)令20mL葡萄酒中二氧化硫的质量为mg,则:
SO2+2H2O+I2═H2SO4+2HI
64g 1mol
mg 0.025L×0.01mol/L
所以,64g:mg=1mol:0.025L×0.0105mol/L,
解得m=0.0168g
故该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为n=$\frac{0.0168g}{0.02L}$=0.84 g/L,
故答案为:0.84.
点评 本题考查物质的制备实验、实验方案设计,为高频考点,侧重于学生的分析能力、实验能力的考查,难度中等,明确实验原理是解本题关键,根据物质的性质分析解答,注意元素化合物知识的积累和灵活运用.

 阅读快车系列答案
阅读快车系列答案| A. | H+、Al3+、Cl-、NO3- | B. | Al3+、Mg2+、SO42-、OH- | ||
| C. | Fe2+、H+、K+、MnO4- | D. | Cu2+、H+、Cl-、HCO3- |
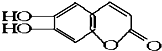 ,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )
,具有抗菌作用.若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为 ( )| A. | 3mol Br2;2mol NaOH | B. | 3mol Br2;4mol NaOH | ||
| C. | 2mol Br2;3mol NaOH | D. | 4mol Br2;4mol NaOH |
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-393.5 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=-890.3 kJ/mol | |
| C. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(g)△H=-1400 kJ/mol |
| A. | 向淀粉溶液中加入稀硫酸,加热一段时间后再加入银氨溶液,水浴加热,检验淀粉是否水解 | |
| B. | 向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热,检验混合物中是否含有甲醛 | |
| C. | 制硝基苯时,将盛有混合液的试管加热,控制温度100-110℃ | |
| D. | 要鉴别己烯中是否混有甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 |
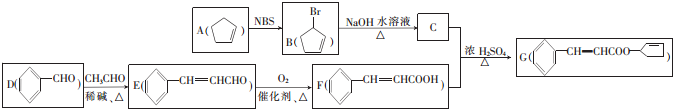
 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaBr,其反应类型为取代反应.
+NaBr,其反应类型为取代反应.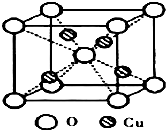 铜是过渡元素.化合物中,铜常呈现+1价或+2价.
铜是过渡元素.化合物中,铜常呈现+1价或+2价. ;
;