题目内容
下列离子方程式书写正确的是( )
| A、氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2C1- |
| B、金属钠投入水中Na+H2O═Na++OH-+H2↑ |
| C、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| D、氯化铁溶液中加氨水3NH3?H2O+Fe3+=3NH4++Fe(OH)3↓ |
考点:离子方程式的书写
专题:
分析:A.电子、电荷不守恒;
B.电子不守恒,原子不守恒;
C.漏写氧化剂水;
D.反应生成氢氧化铝和氯化铵.
B.电子不守恒,原子不守恒;
C.漏写氧化剂水;
D.反应生成氢氧化铝和氯化铵.
解答:
解:A.氯化亚铁溶液中通入氯气的离子反应为2Fe2++Cl2═2Fe3++2C1-,故A错误;
B.金属钠投入水中的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.铝粉投入到NaOH溶液中的离子反应为2Al+2H2O+2OH-═2AlO2-+3H2↑,故C错误;
D.氯化铁溶液中加氨水的离子反应为3NH3?H2O+Fe3+=3NH4++Fe(OH)3↓,故D正确;
故选D.
B.金属钠投入水中的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.铝粉投入到NaOH溶液中的离子反应为2Al+2H2O+2OH-═2AlO2-+3H2↑,故C错误;
D.氯化铁溶液中加氨水的离子反应为3NH3?H2O+Fe3+=3NH4++Fe(OH)3↓,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
将表面已经完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
| A、稀硝酸 | B、硝酸铜 |
| C、稀盐酸 | D、氢氧化钠溶液 |
下列物质中主要成分不是二氧化硅的是( )
| A、硅胶 | B、水晶 |
| C、玛瑙 | D、光导纤维 |
在一密闭容器中充入1mol H2和1mol I2,在一定条件下发生如下反应:H2(g)+I2(g)?2HI(g)
△H<0,下列描述正确的是( )
△H<0,下列描述正确的是( )
| A、保持容器体积不变,向其中充入1mol H2,反应速率加快 |
| B、保持压强不变,向其中充入N2,气体颜色不变 |
| C、保持体积不变,充入1 mol I2,平衡正向移动,气体颜色变浅 |
| D、升高温度,逆反应速率增大,正反应速率减小,平衡逆向移动 |
设阿伏加德常数为NA,则下列说法正确的是:( )
| A、常温常压下,11.2L甲烷中含有的氢原子数为2NA |
| B、标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA |
| C、常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA |
| D、常温下,1L 0.1 mol?L-1AlCl3溶液中含Al3+数为0.1NA |
pH=2的两种一元酸X和Y,体积均为100mL,稀释过程中pH与溶液体积的关系如图所示.分别滴加0.1mol/LNaOH至pH=7,消耗NaOH溶液的体积为VX、VY,下列说法正确的是( )
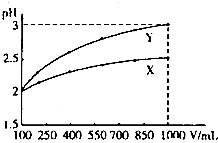

| A、X为弱酸,VX<VY |
| B、Y为强酸,VX>VY |
| C、X为强酸,VX>VY |
| D、Y为弱酸,VX>VY |
 ,核磁共振氢谱显示只有一种化学环境的氢原子,则该烃的结构简式为
,核磁共振氢谱显示只有一种化学环境的氢原子,则该烃的结构简式为