题目内容
在相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法正确的是( )
| A、CO2和SO2中物质的量比为1:1 |
| B、CO2和SO2的密度比为1:1 |
| C、CO2和SO2的物质的量浓度比为11:16 |
| D、CO2和SO2中所含氧原子个数比为16:11 |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算相关物理量,等质量的CO2和SO2气体,物质的量之比与摩尔质量成反比,即16:11.
| m |
| M |
解答:
解:A、CO2和SO2中物质的量比为16:11,故不选;
B、ρ=
,等质量的CO2和SO2气体在体积相同的两个密闭容器内,所以CO2和SO2的密度比为1:1,故选;
C、相一容器中物质的量浓度比等于物质的量之比16:11,故选;
D、每分子CO2和SO2中都含两个氧原子,所以CO2和SO2中所含氧原子个数比等于物质的量之比,即16:11,故选;
故选BD.
B、ρ=
| m |
| V |
C、相一容器中物质的量浓度比等于物质的量之比16:11,故选;
D、每分子CO2和SO2中都含两个氧原子,所以CO2和SO2中所含氧原子个数比等于物质的量之比,即16:11,故选;
故选BD.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,注意把握相关计算公式的推导及应用.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
用铂电极电解100mL HNO3与AgNO3的混合液,通电一段时间后,两极均收集到2.24L气体(标准状况),则原混合液中Ag+的物质的量浓度为( )
| A、1mol/L |
| B、2mol/L |
| C、2.5mol/L |
| D、3mol/L |
下列四种装置(电解质溶液皆为海水)中的铁电极腐蚀速率从快到慢顺序为( )


| A、②③④① | B、②③①④ |
| C、①④③② | D、①②③④ |
下列实验中没用温度计的是( )
| A、蒸馏石油实验 |
| B、酚醛树脂的制备 |
| C、乙醇在浓硫酸作用下发生消去反应 |
| D、硝基苯的制备 |
请根据你所学过的化学知识,判断下列说法中错误的是( )
| A、在使用加酶洗衣粉时先用开水冲泡洗衣粉,这样洗涤效果会增强 |
| B、为防止流感传染,可将教室门窗关闭后,用食醋熏蒸,进行消毒 |
| C、氯化钠是家庭常用的防腐剂,可用来腌制食品 |
| D、家用水壶积存的水垢的主要成分是Mg(OH)2、CaCO3 |
从矿物学资料查得,一定条件下自然界存在如下反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4.下列说法正确的是( )
| A、FeS2只作氧化剂 |
| B、被氧化的硫元素和被还原的硫元素的质量比为3:7 |
| C、生成7 mol Cu2S,有10 mol电子转移 |
| D、氧化剂与还原剂物质的量之比为14:5 |
下列现象表现出浓硫酸脱水性的是( )
| A、盛有浓硫酸的烧杯敞口放置一段时间,质量增加 |
| B、浓硫酸滴在纸上,纸变黑 |
| C、浓硫酸可以用铝制容器盛放 |
| D、热的浓硫酸与木炭反应,放出气体 |
 某无色溶液中只含有下列离子中的某几种:Na+、Mg2+、SO42-、CO32-、Cl-、MnO4-.为了鉴别这些离子,分别取少量溶液进行以下实验:
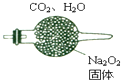
某无色溶液中只含有下列离子中的某几种:Na+、Mg2+、SO42-、CO32-、Cl-、MnO4-.为了鉴别这些离子,分别取少量溶液进行以下实验: 某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.
某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.