题目内容
11.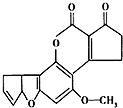 黄曲霉素AFTB1(如图)是污染粮食的真菌霉素.人类的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性.与1mol黄曲霉素起反应的H2或NaOH的最大量分别是( )
黄曲霉素AFTB1(如图)是污染粮食的真菌霉素.人类的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性.与1mol黄曲霉素起反应的H2或NaOH的最大量分别是( )| A. | 6mol,2mol | B. | 7mol,2mol | C. | 6mol,1mol | D. | 7mol,1mol |
分析 在一定条件下能和氢气发生反应的有碳碳不饱和键、羰基、苯环,能和NaOH反应的为酯基水解生成的羧基和酚羟基,据此分析.
解答 解:在一定条件下能和氢气发生反应的有碳碳不饱和键、羰基、苯环,能和NaOH反应的为酯基水解生成的羧基和酚羟基,该分子中含有2个碳碳双键、1个苯环、1个羰基,所以1mol该物质最多能和6mol氢气发生加成反应,酯基水解生成酚羟基和羧基,酚羟基和羧基都能和NaOH反应,所以1mol该物质最多能和2molNaOH反应,故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃、苯环、酯、酮的性质,注意该物质中含有苯环,为易错点.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | H2O和H2O2互为同素异形体 | B. | O2和O3互为同位素 | ||
| C. | 乙醇和二甲醚互为同分异构体 | D. | 12C、13C为同一种核素 |
2.下列电子式中,正确的是( )
| A. | N:::N | B. |  | C. | H+ H+ H+ | D. | Na+ |
19.下列说法正确的是( )
| A. | Ag是短周期元素 | |
| B. | 主族元素的最高价都等于其最外层电子数 | |
| C. | Ne元素属于零族元素 | |
| D. | N的氢化物为H3N |
3.现有0.1mol某金属单质与足量的硫酸溶液反应,放出1.12LH2(标准状况),并转变为具有Ne原子的电子层结构的离子,该金属元素在元素周期表中的位置是( )
| A. | 第三周期第IA族 | B. | 第四周期第IA族 | C. | 第三周期第ⅡA族 | D. | 第四周期第ⅡA族 |
20.草酸与高锰酸钾在酸性条件下能够发生如下反应:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
现用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
(1)该反应中氧化剂是MnO4-.(填化学式)
(2)对比实验Ⅰ和Ⅱ(用Ⅰ~Ⅳ表示,下同),可以研究催化剂对化学反应速率的影响;如果研究温度对化学反应速率的影响,对比实验Ⅰ和Ⅲ.
(3)对比实验Ⅰ和Ⅳ,可以研究浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是确保两实验中总体积相等,可使Ⅰ和Ⅳ中硫酸浓度不同.
现用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其它物质 |
| Ⅰ | 2mL | 20 | / |
| Ⅱ | 2mL | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2mL | 30 | / |
| Ⅳ | 1mL | 20 | 1mL蒸馏水 |
(2)对比实验Ⅰ和Ⅱ(用Ⅰ~Ⅳ表示,下同),可以研究催化剂对化学反应速率的影响;如果研究温度对化学反应速率的影响,对比实验Ⅰ和Ⅲ.
(3)对比实验Ⅰ和Ⅳ,可以研究浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是确保两实验中总体积相等,可使Ⅰ和Ⅳ中硫酸浓度不同.
1.表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置.试用元素符号、离子符号或化学式回答下列问题.
(1)10种元素中,化学性质最不活泼的是Ar(填元素符号).
(2)③④⑤三种元素最高价氧化物对应水化物中,碱性最强的是Ca(OH)2(填化学式),该物质含有的化学键类型是离子键和共价键.
(3)元素⑦的氢化物常温下和元素①的单质反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(4)①和⑦两元素形成四核化合物的电子式是 .
.
(5)元素⑧与元素⑨相比,非金属性较强的是Cl>S(用元素符号表示),下列表述中能证明这一事实的是bd(填序号).
a.与金属化合时,每个硫原子比每个氯原子得电子数多
b.⑨的氢化物比⑧的氢化物稳定
c.一定条件下⑧和⑨的单质都能与氢氧化钠溶液反应
d.最高价氧化物对应水化物酸性⑨比⑧强
(6)元素②的最高价氧化物的水化物与⑤的最高价氧化物的水化物反应的离子方程式为:OH-+Al(OH)3=AlO2-+H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑥ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
| 第4周期 | ② | ④ |
(2)③④⑤三种元素最高价氧化物对应水化物中,碱性最强的是Ca(OH)2(填化学式),该物质含有的化学键类型是离子键和共价键.
(3)元素⑦的氢化物常温下和元素①的单质反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(4)①和⑦两元素形成四核化合物的电子式是
 .
.(5)元素⑧与元素⑨相比,非金属性较强的是Cl>S(用元素符号表示),下列表述中能证明这一事实的是bd(填序号).
a.与金属化合时,每个硫原子比每个氯原子得电子数多
b.⑨的氢化物比⑧的氢化物稳定
c.一定条件下⑧和⑨的单质都能与氢氧化钠溶液反应
d.最高价氧化物对应水化物酸性⑨比⑧强
(6)元素②的最高价氧化物的水化物与⑤的最高价氧化物的水化物反应的离子方程式为:OH-+Al(OH)3=AlO2-+H2O.
 黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物.室温为非活性物质.温度升高后变得活泼.在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:
黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物.室温为非活性物质.温度升高后变得活泼.在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸: