��Ŀ����
һ���¶��£���2L���ܱ������з������·�Ӧ��A��s��+2B��g��?2C��g����H��0����Ӧ������B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����Ӧ��ƽ�����t1��t2��t3��t4ʱ�ֱ�ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2�������й�˵����ȷ���ǣ�������
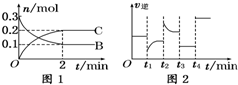

A����Ӧ��ʼ2 min�ڣ�v��B��=
| ||
| B��t1ʱ�ı�����������������¶� | ||
| C��t3ʱ�ı�����������Ǽ�ѹ����ʱc��B������ | ||
| D��t4ʱ������ʹ���˴�������ʱc��B������ |
���㣺��ѧƽ���Ӱ������,��ѧƽ��ļ���
ר�⣺
������A���ٸ���v=��nV��t����v��B����
B������ʱ���淴Ӧ���ʶ����ݴ��жϣ�
C����Ӧǰ����������ʵ������䣬����ѹǿ����������ƽ�ⲻ�ƶ������������С����ʱc��B����ݴ��жϣ�
D��ʹ�ô������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����ʱc��B�����䣬�ݴ��жϣ�
B������ʱ���淴Ӧ���ʶ����ݴ��жϣ�
C����Ӧǰ����������ʵ������䣬����ѹǿ����������ƽ�ⲻ�ƶ������������С����ʱc��B����ݴ��жϣ�
D��ʹ�ô������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����ʱc��B�����䣬�ݴ��жϣ�
���
�⣺A��ͨ��ͼ1��֪��v��B��=0.2mol2L2min=0.05 mol/��L?min������A����
B������ʱ���淴Ӧ���ʶ�����t1ʱ���ʼ�С����B����
C����Ӧǰ����������ʵ������䣬����ѹǿ����������ƽ�ⲻ�ƶ������������С����ʱc��B�����C����
D��ʹ�ô������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����ʱc��B�����䣬��D��ȷ��
��ѡD��
B������ʱ���淴Ӧ���ʶ�����t1ʱ���ʼ�С����B����
C����Ӧǰ����������ʵ������䣬����ѹǿ����������ƽ�ⲻ�ƶ������������С����ʱc��B�����C����
D��ʹ�ô������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����ʱc��B�����䣬��D��ȷ��
��ѡD��
���������⿼�黯ѧ��Ӧ���ʺͻ�ѧƽ���ͼ�����⣬�ѶȲ���ע��ͼ2���������DZ�ʾ�淴Ӧ���ʣ�ע�������仯�淴Ӧ������ʵ�ʱ仯��

��ϰ��ϵ�д�
 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�
�����Ŀ
�����й���Һ����Ũ�ȹ�ϵ��������ȷ���ǣ�������
| A��0.1 mol?L-1NH4Cl��Һ�У�c��NH4+����c��Cl-����c��H+����c��OH-�� |
| B�����е����ʵ���NaClO��NaHCO3����Һ�У�c��HClO��+c��ClO-��=c��HCO3-��+c��H2CO3��+c��CO32-�� |
| C��pH=5.6��CH3COOH��CH3COONa�����Һ�У�c��Na+����c��CH3COO-�� |
| D��25��ʱ��pH=7��NH4Cl��NH3?H2O�����Һ��c��H+��=c��OH-��=c��NH4+��=c��Cl-�� |
 ��֪��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ?mol-1��һ�������£������Ϊ 1L���ܱ������г���1mol CO2��3mol H2�����CO2��CH3OH��g����Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ���ǣ�������
��֪��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.0kJ?mol-1��һ�������£������Ϊ 1L���ܱ������г���1mol CO2��3mol H2�����CO2��CH3OH��g����Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ���ǣ�������| A�������¶���ʹCH3OH���� |
| B����Ӧ�ﵽƽ��״̬ʱ��CO2��ƽ��ת����Ϊ75% |
| C��3 minʱ����CO2��Ũ�ȱ�ʾ������Ӧ���ʵ�����CH3OH��Ũ�ȱ�ʾ���淴Ӧ���� |
| D���ӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ���ʦԣ�H2��=0.075 mol?L-1?min-1 |
����˵�����ʾ����ȷ���ǣ�������
| A�������İ��������Ͱ�����ֱ���ȫȼ�գ����߷ų������� |
| B����C��ʯī����C�����ʯ������H=+1.19 kJ?mol-1��֪�����ʯ��ʯī�ȶ� |
| C����ϡ��Һ�У�H+��aq��+OH-��aq��=H2O��l������H=-57.3 kJ?mol-1��������0.5 mol H2SO4��Ũ�����뺬1 mol NaOH����Һ��ϣ��ų�����������57.3 kJ |
| D����101KPaʱ��1molCH4��ȫȼ������CO2��ˮ�����ų�����������CH4��ȼ���� |
���ж��ڱ���������ȷ���ǣ�������
| A���ױ�ǿ������KMnO4������ |
| B�����ڲ������������ӳɷ�Ӧ |
| C����Ȼ�����͵��Ƚ�����ȡ����Ӧ |
| D������һ����Ҫ���л��ܼ��ɹ㷺Ӧ����������ɫ����� |
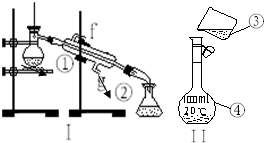 �������������ƣ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�ã�
�������������ƣ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�ã�