题目内容
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气) 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是( )
A.平衡时,物质的量比A∶B∶C=2∶11∶4
B.x值等于4
C.B的平均反应速率为0.04 mol·L-1·min-1
D.A的转化率20%
(1)常温常压下,依据事实,写出下列反应的热化学方程式。
①在25℃、101kPa下,2g甲醇燃烧生成CO2和液态水时放热45kJ。则表示甲醇燃烧热 的热化学方程式为______________________。
的热化学方程式为______________________。
②若适量的N2和O2完全反应,每生成23g NO2需要吸收17kJ热量__________________。
(2)断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ.mol-1)下表是一些键能数据(KJ·mol-1)
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C—H | 414 | C—F | 489 | H—F | 565 | F—F | 158 |
H-H | 436 | H-N | 391 |
①根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)﹦CF4(g)+4HF(g) △H
②根据键能和反应热化学方程式1/2N2(g)+3/2H2(g) =NH3(g ) △H = —46 kJ·mol -1 计算N≡N的键能。
-1 计算N≡N的键能。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256kJ的热量(25℃、101 kPa下测得的热量)。
①该反应的热化学方程式为 。
②又已知H2O(l) =H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。


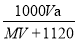 B.
B.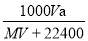 C.
C. D.
D.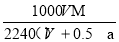
 O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1 C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与
C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与 温度(T)和压强(p)的关系如图所示。下列说法不正确的是
温度(T)和压强(p)的关系如图所示。下列说法不正确的是
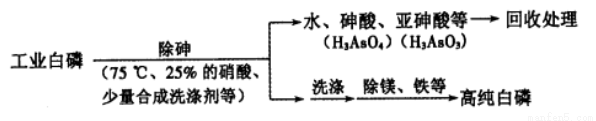
 Ag(NH3)2+(aq) k1=1.10×107
Ag(NH3)2+(aq) k1=1.10×107 2Cl2(g)+2H2O(g),下图是两种投料比[n(HCl):(O2)分别为4:1和2:1]下,反应温度对HCl平衡转化率影响的曲线。则投料比为4:1、溺度为400℃时,平衡混合物中Cl2的体积分数是( )
2Cl2(g)+2H2O(g),下图是两种投料比[n(HCl):(O2)分别为4:1和2:1]下,反应温度对HCl平衡转化率影响的曲线。则投料比为4:1、溺度为400℃时,平衡混合物中Cl2的体积分数是( )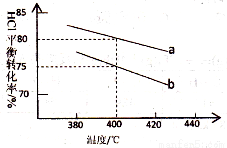
 B.
B.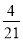 C.
C.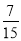 D.
D.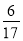
 烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为 ;1mol C60分子中σ键的数目为 个.
烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为 ;1mol C60分子中σ键的数目为 个.