题目内容
3.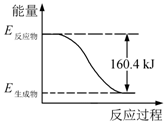 2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室.火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1mol气态水过程中的能量变化图.
2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室.火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1mol气态水过程中的能量变化图.(1)该反应属于放热(填“吸热”或“放热”)反应.
(2)写出该火箭推进器中相关反应的热化学方程式:$\frac{1}{4}$N2H4(l)+$\frac{1}{2}$H2O2(l)=$\frac{1}{4}$N2(g)+H2O(g)△H=-160.4kJ•mol-1.
(3)若该火箭推进器中H2O2有24mol共价键发生断裂,则反应释放出的热量为2566.4kJ.
分析 (1)由图象的,反应物的总能量高于生成物的总能量是放热反应;
(2)N2H4和H2O2完全燃烧生成氮气和1mol气态水放出的热量为160.4kJ•mol-1,据此书写热化学方程式;
(3)1molH2O2有3mol共价键,故24mol共价键,含8molH2O2,由热化学方程式得,0.5molH2O2反应放出160.4 kJ的热量,则8molH2O2反应放出的热量为16×160.4=2566.4 kJ.
解答 解:(1)由图象的,反应物的总能量高于生成物的总能量是放热反应,
故答案为:放热;
(2)N2H4和H2O2完全燃烧生成氮气和1mol气态水放出的热量为160.4kJ•mol-1,故热化学方程式为$\frac{1}{4}$N2H4(l)+$\frac{1}{2}$H2O2(l)=$\frac{1}{4}$N2(g)+H2O(g)△H=-160.4 kJ•mol-1,
故答案为:$\frac{1}{4}$N2H4(l)+$\frac{1}{2}$H2O2(l)=$\frac{1}{4}$N2(g)+H2O(g)△H=-160.4 kJ•mol-1;
(3)1molH2O2有3mol共价键,故24mol共价键,含8molH2O2,由热化学方程式得,0.5molH2O2反应放出160.4 kJ的热量,则8molH2O2反应放出的热量为16×160.4=2566.4 kJ,
故答案为:2566.4.
点评 本题主要考查了热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比,题目难度中等.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
14.化学与科学、技术、社会、环境密切相关.下列说法不正确的是( )
| A. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 | |
| B. | 在食品袋中放人盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 用含橙色酸性重铬酸钾的仪器检验酒驾,利用了乙醇的挥发性和还原性 | |
| D. | 光太阳能电池先将光能转化为化学能,然后再将化学能转化为电能 |
15.有一种军用烟幕弹中装有ZnO、Al粉和C2Cl6,其发烟过程中的化学反应如下:
①3ZnO+2Al→Al2O3+3Zn ②3Zn+C2Cl6→3ZnCl2+2C
下列有关叙述不正确的是( )
①3ZnO+2Al→Al2O3+3Zn ②3Zn+C2Cl6→3ZnCl2+2C
下列有关叙述不正确的是( )
| A. | 反应①是铝热反应 | B. | 反应②是置换反应 | C. | C2Cl6属于卤代烃 | D. | 氧化性:Al<Zn<C |
11.下列事实不能用于判断元素金属性强弱的是( )
| A. | 金属间发生置换反应 | |
| B. | 金属元素的最高价氧化物对应水化物的碱性强弱 | |
| C. | 1mol金属单质在反应中失去电子的多少 | |
| D. | 金属元素的单质与水或酸反应置换出氢气的难易 |
18.下列图象不符合事实是( )
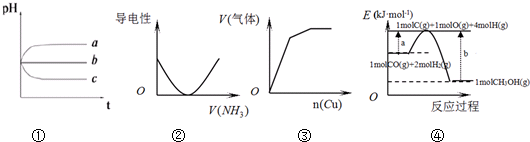

| A. | 图①:pH相同的H2S溶液(a)、稀H2SO4溶液(b)、H2SO3溶液(c)露置于空气中一段时间后,溶液的pH随时间的变化情况 | |
| B. | 图②:表示向乙酸溶液中通入NH3过程中溶液导电性的变化 | |
| C. | 图③:将铜粉加入到一定量浓硝酸中产生的气体与加入铜量的变化情况 | |
| D. | 图④:合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=a-b kJ•mol-1 |
8.下列对一些客观事实和理论解释正确的是( )
| 选项 | 事实 | 理论解释 |
| A | Na 与水反应失去 1 个电子,Mg 与水反应失去 2 个电子 | Na 的金属性比 Mg 强 |
| B | H2S 的还原性比 HCl | S 的非金属性比 Cl |
| C | K3C60在熔融状态下能够导电 | K3C60中含有离子 |
| D | Si 是半导体材料,同主族的 Ge 也 是半导体材料 | ⅣA 元素形成的单质都是半导体材料 |
| A. | A | B. | B | C. | C | D. | D |
15.下列各组物质中,化学键类型完全相同的是( )
| A. | HCl、CaCl2 | B. | H2O2、Na2O2 | C. | NaOH、H2O | D. | CO2、CH4 |
12.下列说法正确的是( )
| A. | 因SiO2不溶于水,故H2SiO3不是SiO2对应的酸,或者说SiO2不是H2SiO3的酸酐 | |
| B. | CO2通入Na2SiO3溶液中可以得到硅酸 | |
| C. | 因为高温时SiO2与Na2CO3反应生成CO2,故硅酸的酸性比碳酸强 | |
| D. | 硅的性质稳定,所以在自然界中可以以游离态存在 |
13.对于可逆反应2A(g)+3B(g)?3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是( )
| A. | 各物质的量浓度之比为c(A):c(B):c(C)=2:3:3 | |
| B. | 正逆反应速率相等且等于零 | |
| C. | 平衡混合物中各物质的量浓度相等 | |
| D. | 单位时间内,若消耗了amolA物质,则同时也消耗了1.5amolC物质 |