题目内容
8.下列对一些客观事实和理论解释正确的是( )| 选项 | 事实 | 理论解释 |
| A | Na 与水反应失去 1 个电子,Mg 与水反应失去 2 个电子 | Na 的金属性比 Mg 强 |
| B | H2S 的还原性比 HCl | S 的非金属性比 Cl |
| C | K3C60在熔融状态下能够导电 | K3C60中含有离子 |
| D | Si 是半导体材料,同主族的 Ge 也 是半导体材料 | ⅣA 元素形成的单质都是半导体材料 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.金属性与失电子能力有关;
B.元素的非金属性越强,其氢化物的还原性越弱;
C.离子化合物在熔融状态下能电离出离子;
D.位于金属与非金属交界处的元素,可作半导体材料.
解答 解:A.金属性与失电子能力有关,越易失电子,金属性越强,与失电子数多少无关,故A错误;
B.元素的非金属性越强,其氢化物的还原性越弱,H2S 的还原性比 HCl,非金属性Cl>S,故B错误;
C.离子化合物在熔融状态下能电离出离子,K3C60在熔融状态下能够导电,说明K3C60在熔融状态下电离出离子属于离子化合物,故C正确;
D.位于金属与非金属交界处的元素,可作半导体材料,第ⅣA元素形成的单质C、金属等不能作半导体材料,故D错误;
故选C.
点评 本题考查了非金属性和金属性强弱的判断,题目难度不大,注意把握非金属性和金属性强弱的判断角度.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
19.氢镍电池放电时的总反应为MH+NiOOH═M+Ni(OH)2.以氢镍电池为电源,能将废水中的CN-转化为CO32-和N2,该装置如图所示.下列说法不正确的是( )
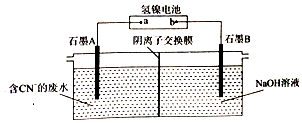

| A. | 电极a为正极 | |
| B. | 负极反应式为MH+OH--e-═H2O+MC | |
| C. | 每消耗1molC N-,理论上导线中通过3mo1e- | |
| D. | 阴极区溶液的PH增大 |
20.在给定的条件下,下列选项中所示的物质间的转化均能一步实现的是( )
| A. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| B. | AgNO3$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$→_{△}^{蔗糖}$ Ag | |
| C. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$ Mg |
16.常温下,下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | 中性溶液:Cu2+、Fe3+、NO3-、I- | |
| B. | 加入硫氰化钾显血红色的溶液:K+、NH4+、Cl-、NO3- | |
| C. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- | |
| D. | 常温下,c(H+)/c(OH-)=1×1012的溶液:K+、AlO2-、CO32-、Na+ |
20.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物叙述正确的是( )
| A. | 一个D216O分子所含的中子数为8 | |
| B. | NH4Cl是只含非金属元素的共价化合物 | |
| C. | HCl的电子式为 | |
| D. | H2S不如HF稳定性强 |
17.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
| A. | H2O2分子中只存在极性键 | B. | NH3的结构式为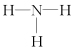 | ||
| C. | HCl的电子式为 | D. | 每个水分子内含有2个氢键 |
18.闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质.软锰矿的主要成分为 MnO2;含少量A12O3和SiO2.现以闪锌矿和软猛矿为原料制备Zn和MnO2,其简化流程如图1(中间产物的固体部分已经略去).
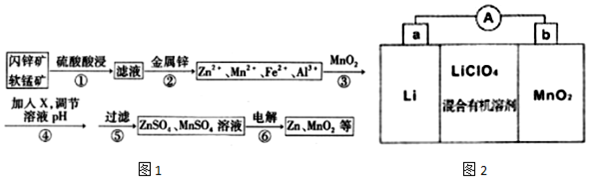
已知:I.矿石中所有金属元素在滤液中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
回答下列问题:
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3MnSO4+Fe2(SO4)3+2S+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③与MnO2发生氧化还原反应的离子方程式MnO2+2Fe2++4H+=2Fe3++Mn 2++2H2O,物质X可以是BD(用字母表示.
A.Cu2(OH)2CO3 B.MnCO3 C.MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是H2SO4(填化学式).
(5)MnO2与Li构成LiMnO2,该电池反应原理如图2所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
①外电路中的电子移动方向是由a极流向b极(填字母).
②写出该锂离子电池的正极电极反应式MnMnO2+e-+Li+=LiMnO2.
(6)已知:25℃时,HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为NaCN+H2S=HCN+NaHS.

已知:I.矿石中所有金属元素在滤液中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3MnSO4+Fe2(SO4)3+2S+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③与MnO2发生氧化还原反应的离子方程式MnO2+2Fe2++4H+=2Fe3++Mn 2++2H2O,物质X可以是BD(用字母表示.
A.Cu2(OH)2CO3 B.MnCO3 C.MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是H2SO4(填化学式).
(5)MnO2与Li构成LiMnO2,该电池反应原理如图2所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
①外电路中的电子移动方向是由a极流向b极(填字母).
②写出该锂离子电池的正极电极反应式MnMnO2+e-+Li+=LiMnO2.
(6)已知:25℃时,HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为NaCN+H2S=HCN+NaHS.
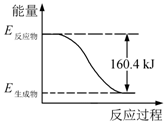 2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室.火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1mol气态水过程中的能量变化图.
2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室.火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1mol气态水过程中的能量变化图.