题目内容
7.某有机物A由C、H、O三种元素组成,在一定条件下,A、B、C、D、E之间的转化关系如图.已知C的蒸气密度是相同条件下氢气的22倍,并可发生银镜反应.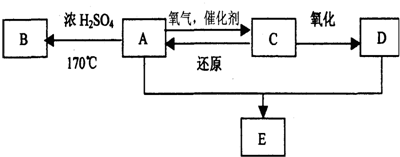
写出下列转化的化学方程式.
(1)B变为高分子
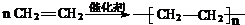 ;
;(2)A+O2→C2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
(3)A+D→ECH3COOH+HOCH2CH3$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
分析 C可发生银镜反应,含有-CHO,C的蒸气密度是相同条件下氢气的22倍,则Mr(C)=22×2=44,含有一个-CHO,剩余基团式量为44-15,剩余基团为甲基,故C为CH3CHO,C氧化生成D为CH3COOH,C发生还原反应生成A为CH3CH2OH,A发生消去反应生成B为CH2=CH2,乙醇与乙酸发生酯化反应生成E为CH3COOCH2CH3,据此解答.
解答 解:C可发生银镜反应,含有-CHO,C的蒸气密度是相同条件下氢气的22倍,则Mr(C)=22×2=44,含有一个-CHO,剩余基团式量为44-15,剩余基团为甲基,故C为CH3CHO,C氧化生成D为CH3COOH,C发生还原反应生成A为CH3CH2OH,A发生消去反应生成B为CH2=CH2,乙醇与乙酸发生酯化反应生成E为CH3COOCH2CH3,
(1)B为乙烯,含有碳碳双键,发生加聚反应生成聚乙烯,化学反应方程式为: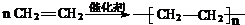 ,
,
故答案为: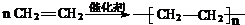 ;
;
(2)A+O2→C是乙醇发生氧化反应生成乙醛,化学反应方程式为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
(3)A+D→E是乙醇与乙酸发生酯化反应生成E为CH3COOCH2CH3,化学反应方程式为:CH3COOH+HOCH2CH3$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:CH3COOH+HOCH2CH3$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸性质与转化,关键是确定C的结构简式,再根据转化关系推断,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.分子式为C6H12O2可以和碳酸氢钠溶液反应产生气体的同分异构体有( )
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 多②12种 |
15.下列说法正确的是( )
| A. | 汽油与水不相溶,可以用裂化汽油萃取溴水中的溴 | |
| B. | 石油含有烷烃、环烷烃、芳香烃,煤含有苯、甲苯、二甲苯等有机物 | |
| C. | 煤的气化、液化是使煤变成清洁能源,减小环境污染的有效途径 | |
| D. | 沸点范围:汽油>煤油>柴油>重油 |
2.青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药.已知:乙醚沸点为35℃.从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为如图:
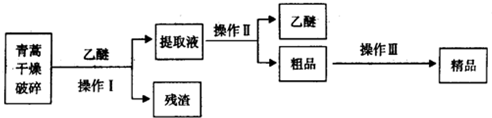
(1)对青蒿进行干燥破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率;
(2)操作I需要的玻璃仪器主要有:烧杯、漏斗、玻璃棒,操作Ⅱ的名称是蒸馏;
(3)操作Ⅲ的主要过程可能是B(填字母);
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算.
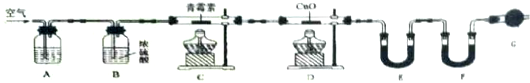
①装置A、E、F中盛放的物质分别是NaOH溶液、CaCl2或P2O5、碱石灰;
②G的作用是防止空气中的CO₂和水蒸气进入F的装置;
③
则测得青蒿素的最简式是C15H22O5,欲确定其分子式,则还需要的物理量为相对分子质量或摩尔质量;
(5)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与C(填字母)具有相同的性质;
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如图所示:
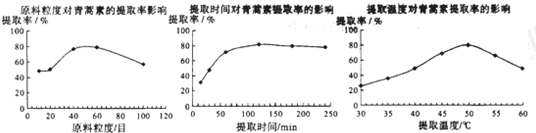
由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为B.
A.80目、100分钟、50℃B.60目、120分钟、50℃C.60目、120分钟、55℃

(1)对青蒿进行干燥破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率;
(2)操作I需要的玻璃仪器主要有:烧杯、漏斗、玻璃棒,操作Ⅱ的名称是蒸馏;
(3)操作Ⅲ的主要过程可能是B(填字母);
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算.

①装置A、E、F中盛放的物质分别是NaOH溶液、CaCl2或P2O5、碱石灰;
②G的作用是防止空气中的CO₂和水蒸气进入F的装置;
③
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
(5)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与C(填字母)具有相同的性质;
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为B.
A.80目、100分钟、50℃B.60目、120分钟、50℃C.60目、120分钟、55℃
12.只有阳离子而没有阴离子的晶体是( )
| A. | 分子晶体 | B. | 金属晶体 | C. | 原子晶体 | D. | 离子晶体 |
19.下列关于化学键的说法不正确的是( )
| A. | 并不是所有物质都含有化学键 | B. | 只有非金属原子间才能形成共价键 | ||
| C. | 单质不可能含有离子键 | D. | 共价化合物中不可能含有离子键 |
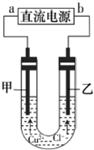
6.用石墨电极电解CuCl2溶液(见图),下列分析正确的是( )

| A. | b端是直流电源的负极 | |
| B. | 用湿润的KI一淀粉试纸检验甲电极产物 | |
| C. | 通电一段时间后,在阴极附近观察到黄绿色气体 | |
| D. | 若将甲电极换成铁棒,乙电极换成铜棒,则可实现在铁棒上镀铜 |
7.黄岩岛海域不仅是重要的海上通道,具有重要的战略地位,而且资源十分丰富,如鱼类、石油、天然气、可燃冰、稀有金属等,经济价值很高.下列有关海水及资源的叙述正确的是( )
| A. | 石油、天然气、乙醇均为不可再生能源 | |
| B. | 天然气的主要成分是CO和H2 | |
| C. | 含氮、磷的大量污水直接排入大海,导致某些浮游生物爆发性繁殖形成赤潮,会造成鱼类的死亡 | |
| D. | 在海水中加入NaOH可提取金属镁 |