题目内容
15.下列说法正确的是( )| A. | 汽油与水不相溶,可以用裂化汽油萃取溴水中的溴 | |
| B. | 石油含有烷烃、环烷烃、芳香烃,煤含有苯、甲苯、二甲苯等有机物 | |
| C. | 煤的气化、液化是使煤变成清洁能源,减小环境污染的有效途径 | |
| D. | 沸点范围:汽油>煤油>柴油>重油 |
分析 A、裂化汽油中含有不饱和烃,不饱和烃能和溴水反应;
B、石油主要由烷烃、环烷烃和各种芳香烃组成;干馏为化学变化,煤干馏后生成苯、甲苯、二甲苯等芳香烃;
C、煤变成清洁能源的有效途径有:煤的气化、液化和干馏;
D、石油分馏时,首先分馏出的是汽油,其次是煤油,再次是柴油、润滑油;
解答 解:A、裂化汽油是石油通过裂化得到,含有不饱和烃,不饱和烃能和溴水发生加成反应,所以裂化汽油不能萃取溴水中的溴,故A错误;
B、石油含有烷烃、环烷烃、芳香烃;干馏为化学变化,煤干馏后生成苯、甲苯、二甲苯等芳香烃,所以煤中不含有苯、甲苯、二甲苯等芳香烃,故B错误;
C、煤的气化、液化是使煤变成清洁能源的有效途径,故C正确;
D、石油分馏时,首先分馏出的是汽油,其次是煤油,再次是柴油、重油,故其沸点:汽油<煤油<柴油<重油,故D错误;
故选C.
点评 本题考查石油的分馏、煤的干馏、气化、液化,应注意裂化汽油中含烯烃,能和溴水中的溴发生加成反应.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
6.下列物质既含有共价键又含有离子键的是( )
| A. | NaCl | B. | Cl2 | C. | HCl | D. | NaOH |
3.化学与生活、社会、科学、技术、环境等息息相关.下列有关说法不正确的是( )
| A. | 12C和14C互为同位素,其中14C可用于文物的年代的鉴定 | |
| B. | 在元素周期表的金属和非金属分界线附近适合寻找半导体材料 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,药学家屠呦呦对青蒿素的提取属于物理变化 | |
| D. | 煤、石油、天然气属于重要的可再生能源,而氢氧燃料电池则是一种能量转换率较高、符合绿色化学理念的新型动力电源 |
20.下列说法不正确的是( )
| A. | CH3CO18OH与CH3OH发生酯化反应达到平衡后,18O仅存在于乙酸、水分子里 | |
| B. | 在体积可变的密闭容器中在一定条件下2molSO2和2molO2发生反应:2SO2(g)+O2═2SO3(g),达到反应最大限度时,容器体积变为反应前的81.25%,则SO2转化率为70% | |
| C. | 对于任何化学反应来说,反应速率越快,反应现象不一定就越明显 | |
| D. | 某同学在用锌片与稀硫酸反应制取氢气时,向反应器中加入少量CuSO4固体(不考虑温度变化),则此时产生H2的化学反应速率加快 |
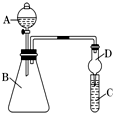 某学习小组同学为探究同周期或同主族元素性质的递变规律,设计了如下系列实验:
某学习小组同学为探究同周期或同主族元素性质的递变规律,设计了如下系列实验: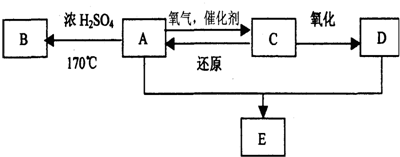
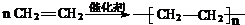 ;
;