题目内容
19.下列关于化学键的说法不正确的是( )| A. | 并不是所有物质都含有化学键 | B. | 只有非金属原子间才能形成共价键 | ||
| C. | 单质不可能含有离子键 | D. | 共价化合物中不可能含有离子键 |
分析 A.稀有气体中不含化学键;
B.金属性较弱的金属与非金属可形成共价键;
C.离子键是阴阳离子之间的静电作用;
D.只含有共价键的化合物属于共价化合物.
解答 解:A.稀有气体是单原子分子,各原子满足稳定结构,所以分子中不存在化学键,只存在分子间作用力,故A正确;
B.金属元素与非金属元素也能形成共价键,如AlCl3为共价化合物,Al与Cl之间形成共价键,故B错误;
C.离子键是阴阳离子之间的静电作用,离子键只存在于离子化合物中,单质不可能含有离子键,故C正确;
D.只含有共价键的化合物属于共价化合物,含有离子键的化合物一定是离子化合物,故D正确;
故选B.
点评 本题考查化学键与化合物的关系,把握化学键形成的一般规律及化学键的判断为解答的关键,侧重分析与应用能力的考查,注意氯化铝为共价化合物,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
9.下列有关化学用语使用正确的是( )
| A. | 次氯酸的结构式:H-Cl-O | B. | 乙烯的结构简式为:CH2CH2 | ||
| C. | CO2的比例模型: | D. | H2F+的电子式: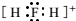 |
14.下列各项叙述中正确的是( )
| A. | 电负性的大小可以作为判断金属性和非金属性强弱的尺度 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| D. | 原子最外层电子排布是5s1的元素,其氢氧化物一定不能溶解氢氧化铝 |
18.下列各对物质中,一定互为同系物的是( )
| A. | C4H8、C2H4 | B. | CH4、C2H5OH | C. | CH3COOH、C3H8 | D. | C2H6、C3H8 |
 某学习小组同学为探究同周期或同主族元素性质的递变规律,设计了如下系列实验:
某学习小组同学为探究同周期或同主族元素性质的递变规律,设计了如下系列实验: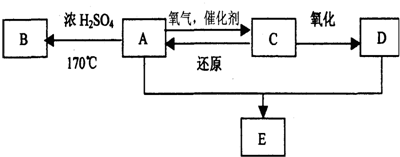
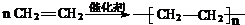 ;
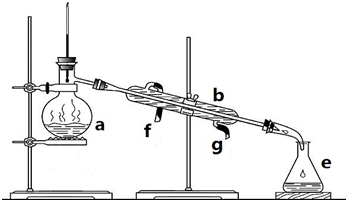
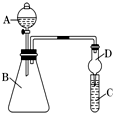
;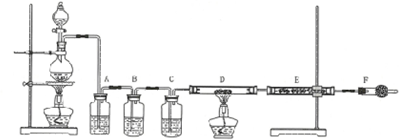 过量的锌与浓硫酸作用的全过程中产生的气体可能有多种.有人认为气体中可能有SO2,也可能有H2.为了说明这两种气体的有无,设计了如图所示的实验装置.
过量的锌与浓硫酸作用的全过程中产生的气体可能有多种.有人认为气体中可能有SO2,也可能有H2.为了说明这两种气体的有无,设计了如图所示的实验装置.