题目内容
如图所示:丁可能是强酸也可能是强碱.
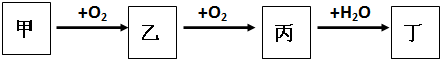
(1)若丙是潜艇的供氧剂,请写出甲与水反应的离子方程式 ;
若等物质的量的甲,乙,丙,丁的固体投入到足量且等量的水中完全反应所得溶液的质量分数由大到小的顺序是 (用化学式表示).
(2)若乙是能使品红溶液褪色的气体,请写出乙→丙的化学反应方程式 ;请写出乙可使氯水褪色的离子方程式 .
(3)若甲可作为制冷剂,请写出甲→乙的化学反应方程式 ;
将等量的铜粉分别与过量浓的丁溶液、稀的丁溶液反应,消耗丁的物质的量:前者 后者,反应中转移的电子总数:前者 后者(填“>”、“=”或“<”)

(1)若丙是潜艇的供氧剂,请写出甲与水反应的离子方程式
若等物质的量的甲,乙,丙,丁的固体投入到足量且等量的水中完全反应所得溶液的质量分数由大到小的顺序是
(2)若乙是能使品红溶液褪色的气体,请写出乙→丙的化学反应方程式
(3)若甲可作为制冷剂,请写出甲→乙的化学反应方程式
将等量的铜粉分别与过量浓的丁溶液、稀的丁溶液反应,消耗丁的物质的量:前者
考点:无机物的推断
专题:推断题
分析:丁可能是强酸也可能是强碱,根据题中各物质转化关系可知,
(1)若丙是潜艇的供氧剂,则丙为过氧化钠,甲为钠,乙为氧化钠,丁为氢氧化钠;
(2)若乙是能使品红溶液褪色的气体,则乙为三氧化硫,丁为硫酸;
(3)若甲可作为制冷剂,则甲为氨气,乙为一氧化氮,丙为二氧化氮,丁为硝酸,据此答题;
(1)若丙是潜艇的供氧剂,则丙为过氧化钠,甲为钠,乙为氧化钠,丁为氢氧化钠;
(2)若乙是能使品红溶液褪色的气体,则乙为三氧化硫,丁为硫酸;
(3)若甲可作为制冷剂,则甲为氨气,乙为一氧化氮,丙为二氧化氮,丁为硝酸,据此答题;
解答:
解:丁可能是强酸也可能是强碱,根据题中各物质转化关系可知,
(1)若丙是潜艇的供氧剂,则丙为过氧化钠,甲为钠,乙为氧化钠,丁为氢氧化钠,甲与水反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,若等物质的量的甲,乙,丙,丁的固体投入到足量且等量的水中完全反应所得溶液中所含溶质的质量甲和丁相等,丙和乙相等,前者是后者的一半,由于钠与水反应产生氢气,所以所得溶液的质量小于氢氧化钠溶于水所得溶液的质量,而氧化钠和过氧化钠与水反应后的溶液的质量相等,所以所得溶液溶质的质量分数由大到小的顺序是Na2O2=Na2O>Na>NaOH,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;Na2O2=Na2O>Na>NaOH;
(2)若乙是能使品红溶液褪色的气体,则乙为三氧化硫,丁为硫酸,所以乙→丙的化学反应方程式为2SO2+O2
2SO3,乙可使氯水褪色的离子方程式为Cl2+SO2+2H2O=2Cl-+SO42-+4H+,
故答案为:2SO2+O2
2SO3;Cl2+SO2+2H2O=2Cl-+SO42-+4H+;
(3)若甲可作为制冷剂,则甲为氨气,乙为一氧化氮,丙为二氧化氮,丁为硝酸,甲→乙的化学反应方程式为4NH3+5O2
4NO+6H2O,将等量的铜粉分别与过量浓硝酸、稀硝酸反应,根据它们的反应的化学方程可知,参加反应的铜与硝酸的物质的量之比前者为1:4,后者为3:8,所以消耗硝酸的物质的量前者大于后者,根据电子得失守恒,由于参加反应的铜的物质的量相等,所以反应中转移的电子总数前者等于后者,
故答案为:4NH3+5O2
4NO+6H2O;>;=;
(1)若丙是潜艇的供氧剂,则丙为过氧化钠,甲为钠,乙为氧化钠,丁为氢氧化钠,甲与水反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,若等物质的量的甲,乙,丙,丁的固体投入到足量且等量的水中完全反应所得溶液中所含溶质的质量甲和丁相等,丙和乙相等,前者是后者的一半,由于钠与水反应产生氢气,所以所得溶液的质量小于氢氧化钠溶于水所得溶液的质量,而氧化钠和过氧化钠与水反应后的溶液的质量相等,所以所得溶液溶质的质量分数由大到小的顺序是Na2O2=Na2O>Na>NaOH,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;Na2O2=Na2O>Na>NaOH;
(2)若乙是能使品红溶液褪色的气体,则乙为三氧化硫,丁为硫酸,所以乙→丙的化学反应方程式为2SO2+O2
| 催化剂 |
| △ |
故答案为:2SO2+O2
| 催化剂 |
| △ |
(3)若甲可作为制冷剂,则甲为氨气,乙为一氧化氮,丙为二氧化氮,丁为硝酸,甲→乙的化学反应方程式为4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
点评:本题主要考查无机物推断、元素单质及其化合物的性质,难度中等,在熟练掌握元素化合物知识的基础上着重考查学生的发散思维、分析判断、逻辑思维以及对无机物知识的综合应用等能力.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2 | |||||
| B、Cu+HNO3(稀)→Cu(NO3)2 | |||||
| C、Cu+AgNO3→Cu(NO3)2 | |||||
D、Cu
|
下列处置、操作或现象的描述中正确的是( )
①漂白粉露置在空气中保存
②金属镁着火时,可用CO2灭火
③让一束光通过胶体,会出现一条光亮的“通路”
④有大量的氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向高处跑.
①漂白粉露置在空气中保存
②金属镁着火时,可用CO2灭火
③让一束光通过胶体,会出现一条光亮的“通路”
④有大量的氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向高处跑.
| A、①② | B、①③ | C、②④ | D、③④ |
关于酚羟基和醇羟基的分析中,错误的是( )
| A、原子组成一样 |
| B、O-H键的化学键类型一样 |
| C、羟基中氢原子活性性不同 |
| D、酚羟基能发生电离,醇羟基也能发生电离 |
物质对应的用途(括号内是用途)错误的是( )
| A、单质硅(光导纤维) |
| B、钠钾合金(原子反应堆导热剂) |
| C、过氧化钠(潜水艇中供氧剂) |
| D、硫酸钡(医疗钡餐) |
下列说法不正确的是( )
| A、分子式为C3H8与C6H14的两种有机物一定互为同系物 |
| B、对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
| C、分子式C4H10表示的物质必是纯净物 |
D、有机物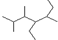 的名称:2,3,5-三甲基-4-乙基庚烷 的名称:2,3,5-三甲基-4-乙基庚烷 |
下列有关电解质溶液中微粒浓度关系正确的是( )
| A、pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
| B、含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C、0.1 mol/L NH4Cl与0.1 mol/L氨水等体积混合(pH>7):c(NH3?H2O)>c(NH4+)>c(Cl-)>c(OH-) |
| D、含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
 科学探究结果的准确性来自于探究活动中研究方法的科学性,研究过程的计划性、研究目的明确性.某学生用如图所示方法研究物质的性质,其中,气体A的主要成分是氯气(含有空气和水蒸气).请回答下列问题:
科学探究结果的准确性来自于探究活动中研究方法的科学性,研究过程的计划性、研究目的明确性.某学生用如图所示方法研究物质的性质,其中,气体A的主要成分是氯气(含有空气和水蒸气).请回答下列问题: