题目内容
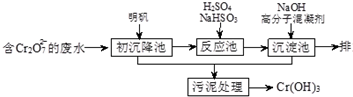
 科学探究结果的准确性来自于探究活动中研究方法的科学性,研究过程的计划性、研究目的明确性.某学生用如图所示方法研究物质的性质,其中,气体A的主要成分是氯气(含有空气和水蒸气).请回答下列问题:
科学探究结果的准确性来自于探究活动中研究方法的科学性,研究过程的计划性、研究目的明确性.某学生用如图所示方法研究物质的性质,其中,气体A的主要成分是氯气(含有空气和水蒸气).请回答下列问题:(1)该项研究(实验)的主要目的是
(2)浓硫酸的作用是
(3)与研究目的直接相关的实验现象是:
考点:实验装置综合
专题:实验设计题
分析:该实验是气体A通过浓硫酸干燥氯气,干燥的氯气通入B,不能使干燥的有色布条褪色,再通入湿润的有色布条中,布条褪色,证明干燥的氯气没有漂白性;氯气有毒,装置中应加上尾气吸收装置,以此来解答.
解答:
解:(1)该实验通过观察干燥氯气与湿氯气分别对有色布条的漂白作用,即该实验目的为比较干燥的氯气和次氯酸(潮湿的氯气)的漂白性(或研究氯气的漂白性实验),故答案为:比较干燥的氯气和次氯酸(潮湿的氯气)的漂白性(或研究氯气的漂白性实验);
(2)浓H2SO4具有吸水性,可吸收水蒸气,在本实验中的作用是吸收气体A中的水、干燥氯气,故答案为:吸收气体A中的水、干燥氯气;
(3)该实验可观察到A瓶中湿氯气在浓硫酸瓶中鼓泡后被干燥、B瓶中干燥的布条不褪色、C瓶中氯气与水生成氯水、有色布条褪色,则与研究目的直接相关的实验现象是B中有色布条不褪色,C中有色布条褪色,
故答案为:B中有色布条不褪色,C中有色布条褪色.
(2)浓H2SO4具有吸水性,可吸收水蒸气,在本实验中的作用是吸收气体A中的水、干燥氯气,故答案为:吸收气体A中的水、干燥氯气;
(3)该实验可观察到A瓶中湿氯气在浓硫酸瓶中鼓泡后被干燥、B瓶中干燥的布条不褪色、C瓶中氯气与水生成氯水、有色布条褪色,则与研究目的直接相关的实验现象是B中有色布条不褪色,C中有色布条褪色,
故答案为:B中有色布条不褪色,C中有色布条褪色.
点评:本题考查实验装置的综合应用及漂白性实验探究,为高频考点,把握B、C装置的对比作用及A中干燥氯气为解答的关键,注意实验目的与现象的联系,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
| A、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1 452 kJ?mol-1 |
| B、CH3OH(l)+1.5O2(g)=CO2(g)+2H2O(g)△H=-725.8 kJ?mol-1 |
| C、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-725.8 kJ?mol-1 |
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=+1 452 kJ?mol-1 |
同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是:①NO和O2,②N2和NO2,③NH3和NO,现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
| A、V1>V2>V3 |
| B、V1>V3>V2 |
| C、V2>V3>V1 |
| D、V3>V1>V2 |
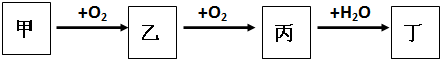
已知:H2(g)+Cl2(s)?2HCl(g)△H=+akJ/mol H2(g)+Cl2(g)?2HCl(g)△H=-dkJ/mol 且a、b、c、d均大于零,则下列说法正确的是( )
且a、b、c、d均大于零,则下列说法正确的是( )
 且a、b、c、d均大于零,则下列说法正确的是( )
且a、b、c、d均大于零,则下列说法正确的是( )| A、断开1molH-Cl键所需的能量为-a-b-c |
| B、b>c,则氢气分子具有的能量高于氯气分子具有的能量 |
| C、Cl2(s)=Cl2(g)△H=+(a+d)kJ?mol-1 |
| D、向1molCl2(g)中通入1molH2(g),发生反应时放热dkJ |
等质量的下列有机物,完全然燃烧需要的氧气的量最多的是( )
| A、苯 | B、甲烷 | C、乙烷 | D、十七烷 |
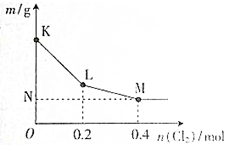 向100mlNaBr和NaI的混合溶液中慢慢通入Cl2(假设Cl2全部反应),使其充分反应后,将所得溶液蒸干、灼烧、得到的固体的质量为m,m与通入的n(Cl2)的关系如图所示,下列说法正确的是( )
向100mlNaBr和NaI的混合溶液中慢慢通入Cl2(假设Cl2全部反应),使其充分反应后,将所得溶液蒸干、灼烧、得到的固体的质量为m,m与通入的n(Cl2)的关系如图所示,下列说法正确的是( )| A、K→L段发生反应的离子方程式为2Br-+Cl2═2Cl-+Br2 |
| B、原溶液中,c(Na+ )=4mol?L-1 |
| C、原溶液中,c(I-)=2mol?L-1 |
| D、M点代表的固体质量为46.8g |