题目内容
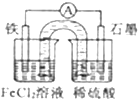 某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.原电池工作一段时间后,下列叙述正确的是( )
某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.原电池工作一段时间后,下列叙述正确的是( )| A、FeCl2溶液中c(Cl-)会增大 |
| B、原电池装置中的盐桥完全可用金属导线代替 |
| C、铁电极上发生了氧化反应,右边溶液的pH减少 |
| D、电子由Fe电极经导线流向石墨电极,再经稀硫酸、盐桥、FeCl2溶液流回Fe电极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铁为负极,被氧化,电极反应为Fe-2e-=Fe2+,石墨为正极,发生还原反应,电极反应为2H++2e-=H2↑,阴离子向负极移动,阳离子向正极移动,结合电极反应解答.
解答:
解:A.Fe为负极,阴离子向负极移动,则FeCl2溶液中c(Cl-)会增大,故A正确;
B.电子不能通过溶液,则原电池装置中的盐桥完不能用金属导线代替,故B错误;
C.右侧电极反应为2H++2e-=H2↑,氢离子浓度减小,则pH增大,故C错误;
D.电子不能通过溶液,故D错误.
故选A.
B.电子不能通过溶液,则原电池装置中的盐桥完不能用金属导线代替,故B错误;
C.右侧电极反应为2H++2e-=H2↑,氢离子浓度减小,则pH增大,故C错误;
D.电子不能通过溶液,故D错误.
故选A.
点评:本题考查原电池知识,侧重于原电池的工作原理的考查,为高考高频考点,注意把握电极反应的判断,把握电极方程式的书写,为解答该类题目的关键,难度不大.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
下列说法正确的是( )
| A、摩尔是物质的质量单位 |
| B、氢气的摩尔质量是2g |
| C、1mol H3O+ 的质量是19g |
| D、气体摩尔体积是指单位物质的量的物质所占的体积 |
用水将pH=3的CH3COOH稀释一倍后,溶液的pH为( )
| A、3 | B、3.15 |
| C、3.3 | D、2.7 |
海水中可以提取镁,其方法是首先使海水中的Mg2+转化为Mg(OH)2沉淀.从经济效益的角度考虑,可在海水中加入的物质是( )
| A、NaOH |
| B、KOH |
| C、CaO |
| D、Na2O |
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素的原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A、X2Y的沸点比X2R高,是因为X2Y分子之间氢键比X2R分子之间的氢键强 |
| B、W与Y形成化合物的分子式为WY2 |
| C、WX4空间构型为正四面体形,WX4分子的稳定性强于甲烷 |
| D、原子半径按Z、W、R、Y、X的顺序依次减小 |
0.1mol/L NH4Cl溶液中,如果要使c (NH4+)接近于0.1mol/L,可采取的措施是( )
| A、加入少量氢氧化钠 |
| B、加入少量盐酸 |
| C、加入少量水 |
| D、加热 |