题目内容
11.下列的叙述中,不正确的是( )| A. | 液氨汽化吸热,故液氨常做食品工厂的制冷剂 | |
| B. | 硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂和阻燃剂 | |
| C. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| D. | 可用冷的浓硝酸迅速除去铝壶底的水垢 |
分析 A、液氨汽化是一个吸热的过程;
B.水玻璃具有耐酸、耐高温等性能;
C.水晶的成分是二氧化硅;
D、铝和酸反应,常温下在浓硫酸、浓硝酸中发生钝化阻止反应进行;
解答 解:A.液氨汽化时能吸收大量的热,故可用作制冷剂,故A正确;
B.水玻璃具有耐酸、耐高温等性能,可用作木材防腐剂和阻燃剂,故B正确;
C.水晶的成分是二氧化硅,不是硅酸盐,故C错误;
D、浓硝酸与铝钝化,不会腐蚀铝壶,和碳酸钙反应溶解水垢,故D正确;
故选C.
点评 本题考查到二氧化硫、水玻璃以及二氧化硅等物质的性质和用途,题目难度不大,学习中注意积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.请选用适当的化学试剂和实验用品,用如图中的实验装置进行实验,证明过氧化钠可作供氧剂.
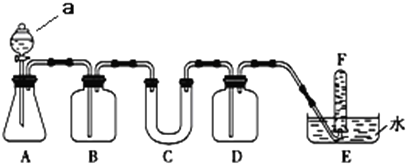
(1)A是制取CO2的装置.仪器a的名称分液漏斗写出A中发生反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)填写表中空格:(请在答题卡上填写)
(3)写出过氧化钠与二氧化碳反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.该反应中氧化剂与还原剂的物质的量之比为1:1
(4)如果实验室将1.5mol过氧化钠与3mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是Na2CO3.

(1)A是制取CO2的装置.仪器a的名称分液漏斗写出A中发生反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)填写表中空格:(请在答题卡上填写)
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | Na2O2 | 与CO2及水蒸气反应,产生O2 |
| D | . |
(4)如果实验室将1.5mol过氧化钠与3mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是Na2CO3.
2.下列说法不正确的是( )
| A. | 12C和14C互为同位素 | |
| B. | 乙醇与二甲醚(CH3-O-CH3)互为同分异构体 | |
| C. | H2O与D2O互为同位素 | |
| D. | 红磷与白磷互为同素异形体 |
19.下列各组元素性质递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数逐渐增多 | |
| B. | P、S、Cl最高正价依次升高 | |
| C. | N、O、F得电子能力逐渐减弱 | |
| D. | Li、Na、K、Rb的金属性依次增强 |
6.下列操作不能在石英坩埚中进行的是( )
| A. | 加热分解NaHCO3 | B. | 加热硫酸铜晶体 | C. | 熔化烧碱 | D. | 加热氯酸钾 |
16.在溶液中能共存,加入OH-有沉淀析出,加入H+能放出气体的是( )
| A. | Mg2+、Na+、Cl-、CO32- | B. | Fe2+、NO3-、Na+、Cl- | ||
| C. | NH4+、K+、AlO2-、SiO32- | D. | Cu2+、NH4+、SO42+、Na+ |
3.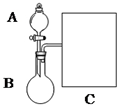 氨水是一种的常用的化学试剂.
氨水是一种的常用的化学试剂.
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少量氨 气.已知:NH3•H2O+CaO═Ca(OH)2+NH3↑.
①生石灰应该装在B(填A或B).
②试从电离平衡角度分析该实验中氨气逸出的原因:CaO与水反应生成Ca(OH)2,溶液中OH-浓度增大,使NH3+H2O?NH4++OH-平衡逆向移动,有利于NH3逸出
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置.
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显.影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二:水浴加热的条件.
②你设计实验验证上述“因素一”,完成下表中内容.
提供试剂:乙醛、2%稀氨水、0.25mol/L NaOH溶液、盐酸、2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
 氨水是一种的常用的化学试剂.
氨水是一种的常用的化学试剂.(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少量氨 气.已知:NH3•H2O+CaO═Ca(OH)2+NH3↑.
①生石灰应该装在B(填A或B).
②试从电离平衡角度分析该实验中氨气逸出的原因:CaO与水反应生成Ca(OH)2,溶液中OH-浓度增大,使NH3+H2O?NH4++OH-平衡逆向移动,有利于NH3逸出
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置.
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显.影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二:水浴加热的条件.
②你设计实验验证上述“因素一”,完成下表中内容.
提供试剂:乙醛、2%稀氨水、0.25mol/L NaOH溶液、盐酸、2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验步骤 | 实验操作 | 预期现象及结论 (步骤1只写现象) |
| 1 | 在A、B两支洁净的试管中各加入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至沉淀恰好溶解,此时制得pH均约为8的银氨溶液. | 先生成白色沉淀 后沉淀溶解 |
| 2 | 往A、B试管加入3滴乙醛,然后在A试管中加1滴NaOH溶液;振荡后将两支试管放在热水浴中温热. | 若A试管比B试管出现的银镜时间短、光亮,则则溶液pH大 反应速率快; 若A试管比B试管出现的银镜时间长,则则溶液pH大 反应速率慢. |
20.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 1mol CH3+(碳正离子)中含有电子数为10NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 1mol乙烷分子含有8NA个共价键 |