题目内容
19.下列各组元素性质递变情况错误的是( )| A. | Li、Be、B原子最外层电子数逐渐增多 | |
| B. | P、S、Cl最高正价依次升高 | |
| C. | N、O、F得电子能力逐渐减弱 | |
| D. | Li、Na、K、Rb的金属性依次增强 |
分析 A、同周期元素的原子,从左到右,最外层电子数依次增多;
B、元素最高正价=最外层电子数;
C、同周期元素的原子,从左到右,非金属性逐渐增强,原子的得电子能力也逐渐增强;
D、同一主族元素,从上到下,金属性依次增强.
解答 解:A、Li、Be、B原子最外层电子数依次为1、2、3,逐渐增多,故A正确;
B、P、S、Cl元素最高正价依次为+5、+6、+7,逐渐升高,故B正确;
C、N、O、F是同周期元素的原子,从左到右,非金属性逐渐增强,得电子能力也逐渐增强,故C错误;
D、Na、K、Rb是同主族元素,从上到下的金属性依次增强,故D正确.
故选C.
点评 本题考查学生元素周期律的应用知识,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目
9.A、B、C都是短周期元素,原子序数依次增大.B是地壳中含量最多的元素;化合物AxBy有多种形式,有的可以导致酸雨;离子化合物CmBn也有不同形式,其中m:n可以是2:1或1:1.下列正确的是( )
| A. | 原子半径由大到小的顺序是:C>B>A | |
| B. | AxBy中A的化合价不可能为+1价 | |
| C. | C与B形成的化合物溶于水都能得到单质B | |
| D. | A、B两元素的气态氢化物可以相互反应 |
10.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A. | 元素Y、Z、W离子具有相同的电子层结构,其半径依次增大 | |
| B. | 元素X与元素Y可以形成两种共价化合物,且这两种化合物只有一种类型的共价键 | |
| C. | 元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XnR | |
| D. | 元素W、R的最高价氧化物对应水化物都是强酸 |
14.下列说法不正确的是( )
| A. | 氯化钠属于离子化合物,只存在Na+、Cl-的离子形式,不存在NaCl分子 | |
| B. | 化学冰袋(硝酸铵、碳酸钠晶体)冷藏食物利用了其反应和溶解吸热的原理 | |
| C. | 血液透析技术利用了胶体与有害物质微粒直径不同的特点 | |
| D. | 酒精检测仪检测司机是否酒后驾车利用了乙醇的还原性 |
11.下列的叙述中,不正确的是( )
| A. | 液氨汽化吸热,故液氨常做食品工厂的制冷剂 | |
| B. | 硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂和阻燃剂 | |
| C. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| D. | 可用冷的浓硝酸迅速除去铝壶底的水垢 |
9.从能量的变化和反应的快慢等角度研究反应:2H2+O2═2H2O.
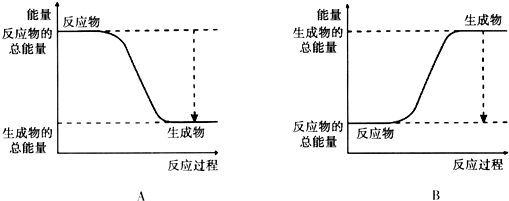
(1)已知该反应为放热反应,下图能正确表示该反应中能量变化的是A.
(2)从断键和成键的角度分析上述反应中能量的变化.已知:化学键的键能:
由此计算2mol H2在氧气中燃烧生成气态水放出的热量484kJ
(3)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为2H2 (g)+O2(g)=2H2O(l)△H=-4QKJ/mol
(4)氢氧燃料电池的总反应方程式为2H2+O2═2H2O.电路中每转移0.2mol电子,标准状况下消耗H2的体积是2.24L.
(1)已知该反应为放热反应,下图能正确表示该反应中能量变化的是A.

(2)从断键和成键的角度分析上述反应中能量的变化.已知:化学键的键能:
| 化学键 | H-H | O=O | H-O |
| 键能kJ•mol-1 | 436 | 496 | 463 |
(3)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为2H2 (g)+O2(g)=2H2O(l)△H=-4QKJ/mol
(4)氢氧燃料电池的总反应方程式为2H2+O2═2H2O.电路中每转移0.2mol电子,标准状况下消耗H2的体积是2.24L.
 现有浓度均为0.1mol•L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
现有浓度均为0.1mol•L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题: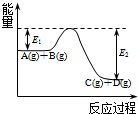 (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.
(1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.