��Ŀ����
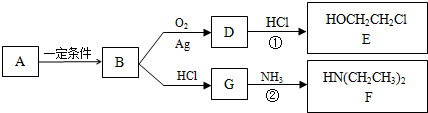
6����ҵ�ϳ������ĺ���������XΪ��Ҫԭ�������ɽ�������PCL{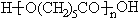 }����ȼ������˫��A���ϳ���·��ͼ��
}����ȼ������˫��A���ϳ���·��ͼ��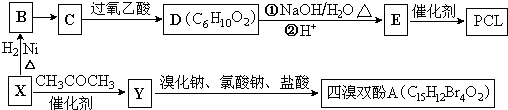
��֪��
��X�������ܶ�����ͬ������H2��47������FeCl3��Һ����ɫ��CΪ
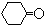
��
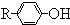 $\stackrel{�廯�ơ��Ȼ��ơ�����}{��}$
$\stackrel{�廯�ơ��Ȼ��ơ�����}{��}$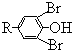
��RCOCH2R��$\stackrel{��������}{��}$RCOOCH2R��
��1��X�ķ���ʽΪC6H6O��B�������ǻ�������
��2��B��C����Ҫ�ķ�Ӧ�Լ���������O2��Cu�����ȣ�C��D�ķ�Ӧ������������Ӧ��
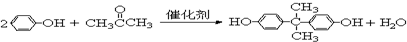
��3��д��X��Y�Ļ�ѧ����ʽ��
 ��
����4��0.5mol����˫��A��һ����������������NaOH��Һ��Ӧ���������5molNaOH��
��5����������������D��ͬ���칹����10�֣������ǿռ��칹����
�ٺ��������������ֹ����� ����ʹ���CCl4��Һ��ɫ ���ܷ���������Ӧ
��6����֪��ϩ��ֱ���Ʊ������������·���Ϊ��
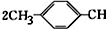 =CH2+2ROH+2CO+O2$\stackrel{һ������}{��}$
=CH2+2ROH+2CO+O2$\stackrel{һ������}{��}$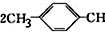 =CHCOOR+2H2O��������ϩΪ�л�ԭ�ϣ�����ͷ�Ӧ������ѡ���ϳɾۺ���Ϳ��
=CHCOOR+2H2O��������ϩΪ�л�ԭ�ϣ�����ͷ�Ӧ������ѡ���ϳɾۺ���Ϳ��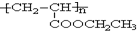 ��д���ϳɸ�Ϳ�ϵķ�Ӧ����ͼ��
��д���ϳɸ�Ϳ�ϵķ�Ӧ����ͼ��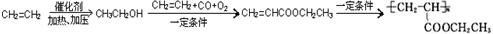 ��
��
���� X�������ܶ�����ͬ������H2��47��������Է�������Ϊ47��2=94����FeCl3��Һ����ɫ��˵�����з��ǻ�����XΪ ��X�����������ӳɷ�Ӧ����BΪ
��X�����������ӳɷ�Ӧ����BΪ ��CΪ
��CΪ ����B������������Ӧ����C��PCLΪE�������۷�Ӧ�����E�ṹ��ʽΪHO��CH2��5COOH��D����ˮ�ⷴӦȻ���ữ�õ�E�������Ϣ��֪D�Ľṹ��ʽΪ
����B������������Ӧ����C��PCLΪE�������۷�Ӧ�����E�ṹ��ʽΪHO��CH2��5COOH��D����ˮ�ⷴӦȻ���ữ�õ�E�������Ϣ��֪D�Ľṹ��ʽΪ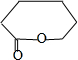 �����������Ϣ��֪��Y�ṹ��ʽΪ
�����������Ϣ��֪��Y�ṹ��ʽΪ ������˫��A�ṹ��ʽΪ
������˫��A�ṹ��ʽΪ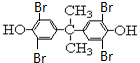 ��
��
��6��һ����������ϩ��ˮ�����ӳɷ�Ӧ����CH3CH2OH��CH3CH2OH��CH2=CH2��CO��O2��Ӧ����CH2=CHCOOCH2CH3��CH2=CHCOOCH2CH3�����Ӿ۷�Ӧ����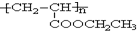 ��
��
��� �⣺X�������ܶ�����ͬ������H2��47��������Է�������Ϊ47��2=94����FeCl3��Һ����ɫ��˵�����з��ǻ�����XΪ ��X�����������ӳɷ�Ӧ����BΪ
��X�����������ӳɷ�Ӧ����BΪ ��CΪ
��CΪ ����B������������Ӧ��PCLΪE�������۷�Ӧ�����E�ṹ��ʽΪHO��CH2��5COOH��D����ˮ�ⷴӦȻ���ữ�õ�E�������Ϣ��֪D�Ľṹ��ʽΪ
����B������������Ӧ��PCLΪE�������۷�Ӧ�����E�ṹ��ʽΪHO��CH2��5COOH��D����ˮ�ⷴӦȻ���ữ�õ�E�������Ϣ��֪D�Ľṹ��ʽΪ �����������Ϣ��֪��Y�ṹ��ʽΪ
�����������Ϣ��֪��Y�ṹ��ʽΪ ������˫��A�ṹ��ʽΪ
������˫��A�ṹ��ʽΪ ��
��
��1��XΪ���ӣ��������ΪC6H6O��BΪ��������
�ʴ�Ϊ��C6H6O����������
��2��B��C����Ҫ�ķ�Ӧ�Լ���������O2��Cu�����ȣ�C����D�ķ�Ӧ��������Ӧ��
�ʴ�Ϊ��O2��Cu�����ȣ�������Ӧ��
��3��X��Y�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4������˫��A�ܺ�NaOH��Һ����ȡ����Ӧ�����ɵķ��ǻ���HBr�ܺ�NaOH�����кͷ�Ӧ��0.5mol����˫��A��һ����������������NaOH��Һ��Ӧ���������5molNaOH��
�ʴ�Ϊ��5��
��5��D�ṹ��ʽΪ ��D��ͬ���칹����������������ٺ��������������ֹ����ţ�����ʹ���CCl4��Һ��ɫ��˵����̼̼˫���� ���ܷ���������Ӧ˵������ȩ�������Կ���ϩ��Ϊ-OOCHȡ����
��D��ͬ���칹����������������ٺ��������������ֹ����ţ�����ʹ���CCl4��Һ��ɫ��˵����̼̼˫���� ���ܷ���������Ӧ˵������ȩ�������Կ���ϩ��Ϊ-OOCHȡ����
��ΪCH3CH=CHCH2CH3��-OOCHȡ����ȡ��������H����3�֣�
��ΪCH2=C��CH3��CH2CH3��-OOCHȡ����ȡ��������H����2�֣�
��ΪCH2=CHCH��CH3��2��-OOCHȡ����ȡ��������H����3�֣�
��ΪCH3CH=C��CH3��2��-OOCHȡ����ȡ�����ϵ�H����2�֣�
�ʷ���������ͬ���칹�干��10�֣�
�ʴ�Ϊ��10��
��6��һ����������ϩ��ˮ�����ӳɷ�Ӧ����CH3CH2OH��CH3CH2OH��CH2=CH2��CO��O2��Ӧ����CH2=CHCOOCH2CH3��CH2=CHCOOCH2CH3�����Ӿ۷�Ӧ����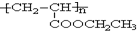 ��������ͼΪ��
��������ͼΪ��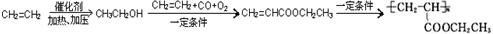 ��
��
�ʴ�Ϊ��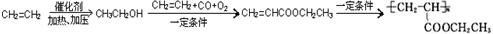 ��
��
���� ���⿼���л��ƶϺ��л��ϳɣ����ؿ���ѧ������������֪ʶ�ۺ�Ӧ��������ע�����Ŀ������Ϣ�����⣬�������չ����ŵ��������ܱ䣬��5������������ͬ���칹�����дΪ�״��㡢�ѵ㣬��Ŀ�Ѷ��еȣ�

| A�� | �ý����Ʒֱ���ˮ���Ҵ���Ӧ���Ƚ�ˮ���Ҵ��������ǻ��⣨-OH���Ļ����ԣ� | |
| B�� | ��ʯī���缫�����Cu��NO3��2��AgNO3�Ļ����Һ��֤������ͭ�����Ľ�����ԣ� | |
| C�� | �ü��ȷ��������Ȼ�淋Ļ��� | |
| D�� | �ü���Na2CO3��Na2SO4ˮ��Һ�����ʵ�飬֤��̼������Ԫ�طǽ����Ե�ǿ���� |
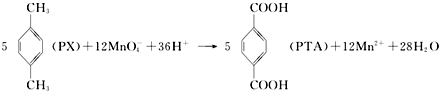
�����й�˵��������ǣ�������
| A�� | PTA�Ǹ÷�Ӧ���������� | |
| B�� | PTA���Ҷ���ͨ���Ӿ۷�Ӧ��������PET���� | |
| C�� | PX���Ӻ��б�����ͬ���칹�廹��3�� | |
| D�� | �÷�Ӧ����1molPX����ת��10mol���� |
| A�� | �����������Һ��ͨ������SO2���壺ClO-+SO2+H2O�THClO+HSO3- | |
| B�� | 0.1mol/LNH4Al��SO4��2��Һ��0.2mol/LBa��OH��2��Һ�������ϣ�Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O | |
| C�� | ��Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO4-+6H++5H2O2�T2Mn2++5O2��+8H2O | |
| D�� | Fe2O3���ڹ����������Һ�У�Fe2O3+6H++2I-�T2Fe2++I2+3H2O |
| A�� | 12gʯī��C60�Ļ��������������Ϊ6NA | |
| B�� | 1L1mol/L�ļ״�ˮ��Һ�к�����ԭ������Ϊ4NA | |
| C�� | ��ӦKIO3+6HI=KI+3H2O+3I2�У�����1molI2ת�Ƶ��ӵ�����Ϊ2NA | |
| D�� | 1.8g2H2O������������ΪNA |
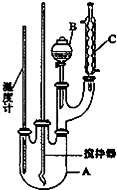 ʵ�����Ʊ��������ķ�Ӧԭ����ʵ��װ�����£�
ʵ�����Ʊ��������ķ�Ӧԭ����ʵ��װ�����£�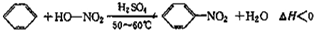
��Ӧ�д��ڵ���Ҫ����Ӧ�У����¶��Ըߵ�����»����ɼ����������
������������
| ���� | ���۵�/�� | ���е�/�� | ���ܶ�/g•cm-3 | ���ܽ��� |
| ���� | ��5.5 | ��80 | ��0.88 | ������ˮ |
| �������� | ��5.7 | ��210.9 | ��1.205 | ��������ˮ |
| ����������� | ��89 | ��301 | ��1.57 | ������ˮ |
| ��Ũ���� | ��83 | ��1.4 | ��������ˮ | |
| ��Ũ���� | ��338 | ��1.84 | ��������ˮ |
�ش��������⣺
��1��ͼ��װ��C������������������
��2�����ƻ����ʱ���ܷ�Ũ������뵽Ũ�����У�˵�����ɣ����ܣ��������Ž���
��3��Ϊ��ʹ��Ӧ��50�桫60���½��У����õķ�����ˮԡ���ȣ���Ӧ��������ȴ�����º�A��Һ����Ǵ������������������ʻ�ɫ��ԭ��������Ũ����ֽ������NO2�������ᣩ�����ʣ�
��4����ϴ�Ӳ����У��ڶ���ˮϴ��������ϴȥ������NaOH�����ɵ��Σ�
��5�������������У����������ķе����140�棬Ӧѡ�ÿ��������ܣ���ѡ��ˮֱ�������ܵ�ԭ��������ֱ��������ͨˮ��ȴʱ�����²���������ը�ѣ�
��6����ʵ�����õ���������������72.06%��
| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/��g•L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |
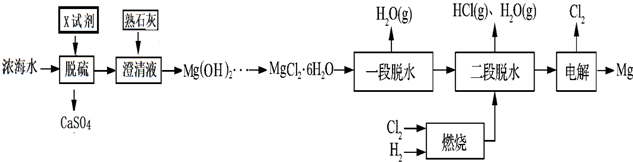
��ش���������
��1��Ũ��ˮ��Ҫ���е��������������ʵ���Ũ����С����SO42-�������������У�����ѭ��ʹ�õ�������Cl2��HCl��
��2���ڸù��չ����У�X�Լ��Ļ�ѧʽΪCaCl2��
��3����һ����ˮ��Ŀ�����Ʊ�MgCl2•2H2O����������ˮ����Ŀ�����Ʊ����ԭ�ϣ�����MgCl2•6H2Oֱ�Ӽ�����ˮ���������Mg��OH��Cl�������ԭ���к���Mg��OH��Cl�����ʱMg��OH��Cl������������Mg��Ӧ��ʹ�����������MgO�ۻ�Ĥ�����͵��Ч�ʣ�����MgO�Ļ�ѧ����ʽΪ2Mg��OH��Cl+Mg=MgCl2+2MgO+H2����
��4�����Ƶ�Mg��OH��2�Ĺ�����Ũ��ˮ��������Ϊ80%����Mg��OH��2����������ˮ���Ƶõ��ԭ�ϵĹ�����þԪ�ص�������Ϊ90%����1m3Ũ��ˮ�ɵá�������ˮ����ĵ��ԭ������Ϊ82080g��
��5����LiCl-KCl������Ϊ����ʵ�Mg-V2O5�����ս�������ij��õ�Դ���õ�ص��ܷ�ӦΪ��Mg+V2O5+2LiCl MgCl2+V2O4•Li2O �õ�ص�������ӦʽΪV2O5+2Li++2e-=V2O4•Li2O��
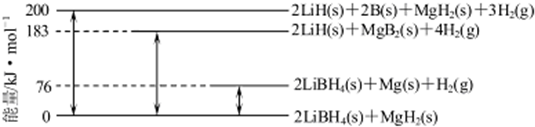
��6��Mg�Ͻ�����Ҫ�Ĵ�����ϣ�2LiBH4/MgH2��ϵ�����ʱ�ʾ��ͼ���£���
Mg��s��+2B��s�� MgB2��s����H=-93kJ/mol��
 ��ƣ�EPABA���ǰ�ɫ��ĩ��ζ����飬�������Ҵ���������ˮ���Ǿֲ�����ҩ��������������ֹʹ������ʹ�ȣ���������ĺϳ�·�����£���Na2Cr2O7��һ��ǿ��������
��ƣ�EPABA���ǰ�ɫ��ĩ��ζ����飬�������Ҵ���������ˮ���Ǿֲ�����ҩ��������������ֹʹ������ʹ�ȣ���������ĺϳ�·�����£���Na2Cr2O7��һ��ǿ�������� +RCl$\stackrel{AlCl_{3}}{��}$
+RCl$\stackrel{AlCl_{3}}{��}$ +HCl
+HCl $��_{HCl}^{Sn}$
$��_{HCl}^{Sn}$
 $\stackrel{��CH_{3}CO��_{2}O}{��}$
$\stackrel{��CH_{3}CO��_{2}O}{��}$
 ��
�� ��
�� ��
��
 $\stackrel{��ԭ}{��}$
$\stackrel{��ԭ}{��}$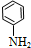 ��
��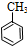 ���ױ���$��_{ŨH_{2}SO_{4}}^{ŨHNO_{3}}$��$\stackrel{����}{��}$��$��_{��}^{E}$
���ױ���$��_{ŨH_{2}SO_{4}}^{ŨHNO_{3}}$��$\stackrel{����}{��}$��$��_{��}^{E}$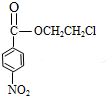 $\stackrel{��ԭ}{��}$��$��_{��}^{F}$
$\stackrel{��ԭ}{��}$��$��_{��}^{F}$ ����³����
����³����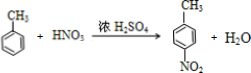 ����Ӧ�۵Ļ�ѧ����ʽ�ǣ����������ֺ��������ţ���
����Ӧ�۵Ļ�ѧ����ʽ�ǣ����������ֺ��������ţ���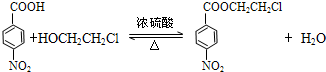 ��
��