题目内容
14.将一定量的Fe和Fe2O3的混合物放入250mL 1.8mol•L-1的硝酸溶液中,当固体混合物完全溶解后,在标准状况下生成1.12LNO(HNO3的还原产物仅此一种),再向反应后的溶液中加入1.0mol?L-1NaOH溶液,若要使铁元素完全沉淀,所加入的NaOH溶液的体积至少应为( )| A. | 300mL | B. | 400mL | C. | 450mL | D. | 500mL |
分析 反应中硝酸体现两种性质,一是酸性,以NO3-离子存在溶液中,另一种是氧化性,被还原为NO,加入NaOH后使铁元素完全沉淀下来,此时溶液的溶质为硝酸钠,根据N元素守恒可知n(NaOH)=n(NO3-)=n(HNO3)-n(NO),再根据V=$\frac{n}{c}$计算.
解答 解:当所加入的NaOH恰好使铁元素沉淀,此时溶液为硝酸钠溶液,根据N元素守恒:n(NaOH)=n(NO3-)=n(HNO3)-n(NO)=0.25L×1.8mol/L-$\frac{1.12L}{22.4L/mol}$=0.4mol,
所以V(NaOH)=$\frac{0.4mol}{1mol/L}$=0.4L=400mL,
故选B.
点评 本题考查有关混合物的计算,题目难度中等,判断溶液中溶质为硝酸钠是关键,再利用N原子守恒计算.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
4.有下列两组命题
B组中命题正确,且能用A组命题加以正确解释的是( )
| A组 | B组 |
| Ⅰ.H2O分子间存在氢键,H2S则无 | ①H2O比H2S稳定 |
| Ⅱ.晶格能NaI比NaCl小 | ②NaCl比NaI熔点高 |
| Ⅲ.晶体类型不同 | ③N2分子比磷的单质稳定 |
| Ⅳ.元素第一电离能大小与原子外围电子排布有关,不一定像电负性随原子序数递增而增大 | ④同周期元素第一电离能大的,电负性不一定大 |
| A. | Ⅰ① | B. | Ⅱ② | C. | Ⅲ③ | D. | Ⅳ④ |
5.如图为铜锌原电池示意图,下列说法正确的是( )
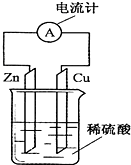

| A. | 锌片上有气泡产生 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电流由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
2.下列实验装置能达到实验目的,且实验装置无明显错误的是(夹持仪器未画出)( )
| A. | 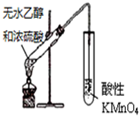 A装置用于检验乙醇发生消去反应的产物 | |
| B. | 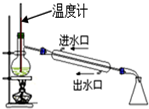 B装置可用于分离乙醇和丙三醇形成的混合物 | |
| C. | 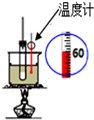 C装置用于实验室制硝基苯 | |
| D. | 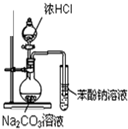 D装置可证明酸性:盐酸>碳酸>苯酚 |
9.高硬度的水对生活和生产都有危害,常需软化处理以降低硬度.下列方法不能降低硬度的是( )
| A. | 过滤 | B. | 离子交换法 | C. | 蒸馏 | D. | 加入软化药剂 |
19.下列分离或提纯物质的方法正确的是( )
| A. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| C. | 用渗析的方法精制Fe(OH)3胶体 | |
| D. | 用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 |
6.下列操作错误的是( )(填序号)
| A. | 用蒸发皿进行加热蒸发实验时,不需要垫石棉网 | |
| B. | 蒸馏时,应将温度计水银球插入液面以下 | |
| C. | 闻气味时,应用手在容器口轻轻扇动,使少量气体飘入鼻孔中 | |
| D. | 使用分液漏斗和容量瓶时,都要首先检查是否漏水 | |
| E. | 分液时,先把分液漏斗中上层液体从上口倒出,再把下层液体从下口放出 |
3.分子式为C7H14O2的有机物Q,在稀硫酸溶液加热可转化为乙醇与另一种酸性物质,则Q的结构最多有( )
| A. | 6种 | B. | 4种 | C. | 3种 | D. | 2种 |
4.下列过程中,不可逆的是( )
| A. | 蛋白质的盐析 | B. | 酯的酸催化水解 | C. | 蛋白质的变性 | D. | 氯化铁的水解 |