题目内容
3.下列物质中属于电解质的是( )| A. | 二氧化碳 | B. | 银 | C. | 烧碱溶液 | D. | NaCl |
分析 电解质是在水溶液中或熔融状态下能导电的化合物,非电解质是在水溶液中和熔融状态下都不能导电的化合物,无论电解质还是非电解质都必须是化合物.
解答 解:A、二氧化碳在熔融状态下不导电,在水溶液中导电和其本身无关,故二氧化碳为非电解质,故A错误;
B、银是单质,故既不是电解质也不是非电解质,故B错误;
C、烧碱溶液是混合物,故既不是电解质也不是非电解质,故C错误;
D、氯化钠在水溶液中和熔融状态下均能导电,故为电解质,故D正确.
故选D.
点评 本题考查了电解质的概念,难度不大,注意电解质本身不一定导电,导电的不一定是电解质.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
13.在一定温度下的密闭容器中,发生反应:A(s)+2B(g)═2C(g)+D(g),下列说法正确的是( )
| A. | 保持体积不变充入He气,体系压强增大,平衡逆向移动 | |
| B. | 保持压强不变充入He气,因为体系压强不变,所以平衡不移动 | |
| C. | 其它条件不变,向体系中加入A,A的转化率减小,B的转化率增大 | |
| D. | 其它条件不变,改变体积使压强改变,逆方向的速率改变的程度大于正方向 |
14.下列各组物质性质的比较中,错误的是( )
| A. | 还原性:HF<HCl<H2S | B. | 金属性:Na>Mg>Be | ||
| C. | 非金属性:F>Cl>S | D. | 离子半径:Al3+>Mg2+>F- |
8.在水溶液中能大量共存的一组离子是( )
| A. | Na+、Al3+、Cl-、CO32- | B. | H+、Na+、Fe2+、MnO4- | ||
| C. | K+、Ca2+、Cl-、CO32- | D. | K+、NO3-、OH-、SO42- |
15.下列离子方程式的书写正确的是( )
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | NaHCO3溶液与NaOH溶液反应:2OH-+2HCO3-═2 CO32-+H2O | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 钠和冷水反应 2Na+2H2O═2Na++2OH-+H2↑ |
12.下列有机物命名正确的是( )
| A. |  2-乙基丙烷 | B. | CH3CH2CH2OH 1-丁醇 | ||
| C. |  2-氯-2-甲基丙烷 | D. |  2-甲基-2-丙烯 |
13.下列物质的用途中,不正确的是( )
| A. | Na2O作呼吸面具中的供氧剂 | B. | 小苏打做发酵粉 | ||
| C. | 镁合金用于制造汽车、飞机、火箭 | D. | 漂白粉做消毒剂 |
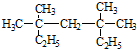 系统命名法为3,3,5,5-四甲基庚烷,
系统命名法为3,3,5,5-四甲基庚烷, ,
,