题目内容
饱和氯水久置后,溶液中的各种粒子:①Cl2 ②H2O ③Cl- ④HClO ⑤H+减少的是( )
| A、①②④ | B、①②③ |
| C、①④ | D、②④ |
考点:氯气的化学性质
专题:卤族元素
分析:氯气溶于水,部分氯气与水反应生成氯化氢和次氯酸,部分以氯气分子形式存在,次氯酸不稳定受热易分解,据此解答.
解答:
解:氯气溶于水,部分以氯气分子形式存在,部分氯气与水反应生成氯化氢和次氯酸,方程式为:Cl2+H2O HCl+HClO,氯化氢为强电解质完全电离出氢离子和氯离子,次氯酸为弱电解质部分电离出氢离子和次氯酸根离子,所以新制氯水中含有:所以新制的氯水中含有三种分子:Cl2、H2O、HClO,四种离子:H+、Cl-、ClO-及少量OH-;
次氯酸不稳定受热易分解,2HClO═2HCl+O2↑,促使Cl2+H2O?HCl+HClO平衡向正向移动,HClO分解导致了Cl2的不断反应,最后变成了HCl溶液,所以减少的是①Cl2、②H2O、④HClO;
故选:A.
次氯酸不稳定受热易分解,2HClO═2HCl+O2↑,促使Cl2+H2O?HCl+HClO平衡向正向移动,HClO分解导致了Cl2的不断反应,最后变成了HCl溶液,所以减少的是①Cl2、②H2O、④HClO;
故选:A.
点评:本题考查了新制氯水和久制氯水的区别,明确氯水的成分与性质是解题关键,题目难度不大,注意对基础知识的积累.

练习册系列答案
相关题目
下列气体中,可溶于水的无色气体是( )
| A、N2 |
| B、NO |
| C、NO2 |
| D、NH3 |
在铜-锌-硫酸构成的原电池中,经过一段时间的工作后,下列说法正确的是( )
| A、锌片是负极,铜片上有气泡冒出 |
| B、电流方向是从锌片流向铜片 |
| C、溶液中硫酸的物质的量不变 |
| D、电解液的pH保持不变 |
被誉为“光纤之父”的科学家高锟荣获2009年诺贝尔化学奖.下列叙述不正确的是( )
| A、SiO2是生产光导纤维和粗硅的主要原料 |
| B、工艺师利用盐酸刻蚀石英制作艺术品 |
| C、SiO2与CO2都属于酸性氧化物,都不能与酸反应 |
| D、水晶的主要成分是SiO2 |
下列说法正确的是( )
| A、3p3表示3p能级有三个轨道 |
| B、同一原子中,2p、3p、4p能级的轨道数依次增多 |
| C、冰和固体碘晶体中的相互作用力不相同 |
D、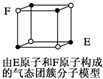 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
已知热化学方程式:SO2(g)+
O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| 1 |
| 2 |
| A、等于196.64kJ?mol-1 |
| B、等于196.64 kJ |
| C、小于196.64kJ |
| D、大于196.64kJ |