题目内容
请参考题中图表,已知E1=134kJ?mol-1、E2=368kJ?mol-1,根据要求回答问题:

(1)图Ⅰ是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是 (填“增大”、“减小”或“不变”,下同),△H的变化是 .请写出NO2和CO反应的热化学方程式: .
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
O2(g)═CO2(g)+2H2(g)△H=-192.9kJ?mol-1
又知③H2O(g)═H2O(l)△H=-44kJ?mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为 .
(3)如表所示是部分化学键的键能参数:
已知白磷的燃烧热为d kJ?mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x= kJ?mol-1(用含a、b、c、d的代表数式表示).

(1)图Ⅰ是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
| 1 |
| 2 |
又知③H2O(g)═H2O(l)△H=-44kJ?mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为
(3)如表所示是部分化学键的键能参数:
| 化学键 | P-P | P-O | O═O | P═O |
| 键能/kJ?mol-1 | a | b | c | x |
考点:反应热和焓变,热化学方程式,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:(1)加入催化剂能降低反应所需的活化能,但是不改变反应物的总能量和生成物的总能量,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(2)依据热化学方程式,利用盖斯定律进行计算;
(3)白磷燃烧的方程式为P4+5O2=P4O10,根据化学键的断裂和形成的数目进行计算.
(2)依据热化学方程式,利用盖斯定律进行计算;
(3)白磷燃烧的方程式为P4+5O2=P4O10,根据化学键的断裂和形成的数目进行计算.
解答:
解:(1)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ?mol-1,
故答案为:减小;不变;NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ?mol-1;
(2)利用盖斯定律进行计算,
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
O2(g)=CO2(g)+2H2(g)△H=-192.9kJ?mol-1
又知 ③H2O(g)=H2O(l)△H=-44kJ/mol
依据盖斯定律计算(②×3-①×2+③×2)×
得到CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-726 KJ/mol;
故答案为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-726 KJ/mol;
(3)白磷燃烧的方程式为P4+5O2=P4O10,1mol白磷完全燃烧需拆开6mol P-P、5mol O=O,形成12molP-O、4mol P=O,
所以12mol×bkJ/mol+4mol×xkJ/mol-(6mol×a kJ/mol+5 mol×c kJ/mol)=dkJ/mol,
x=
kJ/mol,
故答案为:
.
故答案为:减小;不变;NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ?mol-1;
(2)利用盖斯定律进行计算,
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
| 1 |
| 2 |
又知 ③H2O(g)=H2O(l)△H=-44kJ/mol
依据盖斯定律计算(②×3-①×2+③×2)×
| 1 |
| 2 |
| 3 |
| 2 |
故答案为:CH3OH(g)+
| 3 |
| 2 |
(3)白磷燃烧的方程式为P4+5O2=P4O10,1mol白磷完全燃烧需拆开6mol P-P、5mol O=O,形成12molP-O、4mol P=O,
所以12mol×bkJ/mol+4mol×xkJ/mol-(6mol×a kJ/mol+5 mol×c kJ/mol)=dkJ/mol,
x=
| 6a+5c+d-12b |
| 4 |
故答案为:
| 6a+5c+d-12b |
| 4 |
点评:本题考查较为综合,题目难度中等,本题注意热化学方程式的书写方法和计算应用,注意焓变计算和物质聚集状态的标注,学习中要准确把握,另外注意反应热的计算,特别是注意分析白磷的氧化磷的分子结构,正确判断共价键的类型和数目.

练习册系列答案
相关题目
为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg
,则下列叙述正确的是( )
| c(H+) |
| c(OH-) |
| A、中性溶液的AG=1 |
| B、酸性溶液的AG<0 |
| C、常温下0.lmol/L氢氧化钠溶液的AG=12 |
| D、常温下0.lmol/L盐酸溶液的AG=12 |
 有一反应,由X与Y化合生成Z.其反应如右:2X+3Y=2Z,反应物X与生成物Z的质量关系如图.下列说法正确的是( )
有一反应,由X与Y化合生成Z.其反应如右:2X+3Y=2Z,反应物X与生成物Z的质量关系如图.下列说法正确的是( )| A、有4g的Z生成时,则消耗Y 6g |
| B、X、Y、Z的摩尔质量之比为3:2:6 |
| C、2mol X质量与3mol Y质量之和等于2mol Z的质量 |
| D、消耗2mol X时,在标准状况下,生成Z的体积为44.8L |
下列叙述正确的是( )
| A、原子半径:P>S>Cl>H |
| B、热稳定性:NH3>PH3>H2S>HCl |
| C、酸性:HClO4>H2SiO3>H3PO4>H2CO3 |
| D、元素非金属性:F>O>N>C |
已知热化学方程式:2H2(g)+O2(g)=2H2O(g)△H1=-483.6kJ/mol,则对于热化学方程式:2H2O(l)=2H2(g)+O2(g)△H2=b,下列说法正确的是( )
| A、热化学方程式中化学计量数表示分子个数 |
| B、该反应的△H2=+483.6 kJ/mol |
| C、形成2mol H-O键放出能量比断2mol H-H及1mol O=O键所需能量多483.6kJ |
| D、|△H2|>|△H1| |
 ①图象中曲线
①图象中曲线
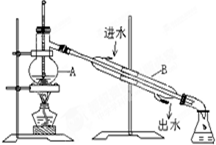 图中装置中仪器的名称:
图中装置中仪器的名称: