题目内容
18.下列各物质相互反应后,再向得到的溶液中滴入NaOH溶液,能直接生成红褐色沉淀的是( )| A. | 氯水和氯化亚铁溶液 | B. | 铁屑和氯化铜溶液 | ||
| C. | 铁屑和过量稀硫酸 | D. | 过量铁屑和氯化铁溶液 |
分析 根据向所得的溶液中滴入NaOH溶液,能直接生成红褐色沉淀,即直接生成Fe(OH)3,则说明各物质相互反应后生成Fe3+.据此分析.
解答 解:向所得的溶液中滴入NaOH溶液,能直接生成红褐色沉淀,即直接生成Fe(OH)3,则说明各物质相互反应后生成Fe3+.
A、氯水和氯化亚铁溶液发生反应:2FeCl2+Cl2=2FeCl3,有Fe3+生成,故A符合题意;
B、铁屑和氯化铜溶液反应生成氯化亚铁:CuCl2+Fe=FeCl2+Cu,无Fe3+生成,故B不符合题意;
C、由于稀硫酸是非氧化性酸,氧化性较弱,故铁屑和过量稀硫酸反应生成的是FeSO4,无Fe3+生成,故C不符合题意;
D、过量的铁屑和氯化铁溶液反应:Fe+2FeCl3=3FeCl2,无Fe3+生成,故D不符合题意.
故选A.
点评 本题考查了物质反应后铁的价态和Fe3+与碱的反应,难度不大,掌握物质间的反应来分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.用NA表示阿伏加德罗常数的值,下列叙述中错误的是( )
| A. | 常温常压下,28 g N2所含有的原子数目为2NA | |
| B. | 室温下,22.4 L的 H2中所含分子数为NA | |
| C. | 标准状况下,1 mol H2O所占的体积约为22.4 L | |
| D. | 常温常压下,24 g Mg与足量的盐酸完全反应转移的电子数为NA |
9.下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),反应结果并不改变的是( )
| A. | Na和O2 | B. | Cu和硝酸 | C. | Cu和硫酸 | D. | Al和NaOH |
6.下列有关化学实验的叙述正确的是( )
| A. | NaOH 溶液保存在带玻璃塞的试剂瓶中 | |
| B. | 配制FeCl2 溶液时,通常向溶液中加入少量Fe 粉 | |
| C. | Cl2 和SO2 都有漂白作用,将Cl2 和SO2 等体积混合后可使品红溶液更快褪色 | |
| D. | 配制物质的量浓度的溶液,定容时仰视刻度线会使所配制的溶液浓度偏高 |
3.将有机物的混合物在一定条件下反应:①甲醇与乙醇的混合物与浓硫酸加热得醚;②乙烷与氯气光照下取代;③氨基乙酸和丙氨酸生成二肽;④苯和液溴、Fe粉反应.所生成的有机物的种类由多到少的顺序是( )
| A. | ③②④① | B. | ③②①④ | C. | ②③①④ | D. | ①②③④ |
10.下列有关工业合成氨的说法不能用平衡移动原理解释的是( )
| A. | 不断补充氮气和氢气 | |
| B. | 选择20MPa-50MPa的高压 | |
| C. | 及时液化分离氨气 | |
| D. | 选择500℃左右的高温同时使用铁触媒做催化剂 |
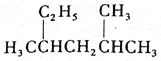 2,4-二甲基己烷
2,4-二甲基己烷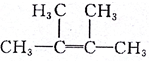 2,3-二甲基-2-丁烯
2,3-二甲基-2-丁烯