题目内容
(1)标准状况下 L二氧化碳中所含的氧原子数与0.8molH2O中所含的氧原子数相等.
(2)质量相同的H2、NH3、SO2、O2四种气体中,含有分子数目最少的是 .
(3)在 mL 0.2mol?L-1NaOH溶液中含4g NaOH溶质.
(2)质量相同的H2、NH3、SO2、O2四种气体中,含有分子数目最少的是
(3)在
考点:物质的量的相关计算
专题:计算题
分析:(1)每个CO2分子中含有两个O原子,每个H2O分子中含有一个O原子,要使CO2、H2O中O原子的个数相等,则n(CO2):n(H2O)=1:2,n(H2O)=0.8mol,则n(CO2)=0.4mol,再根据V=nVm计算二氧化碳体积;
(2)根据N=
NA知,相同质量的不同气体中分子数之比等于其摩尔质量反比;
(3)根据V=
=
计算溶液体积.
(2)根据N=
| m |
| M |
(3)根据V=
| n |
| C |
| ||
| C |
解答:
解:(1)每个CO2分子中含有两个O原子,每个H2O分子中含有一个O原子,要使CO2、H2O中O原子的个数相等,则n(CO2):n(H2O)=1:2,n(H2O)=0.8mol,则n(CO2)=0.4mol,二氧化碳体积V=nVm=0.4mol×22.4L/mol=8.96L,故答案为:8.96;
(2)根据N=
NA知,相同质量的不同气体中分子数之比等于其摩尔质量反比,H2、NH3、SO2、O2四种气体的摩尔质量分别是2g/mol、17g/mol、64g/mol、32g/mol,摩尔质量最大的是SO2,则分子数最少的是SO2,故答案为:SO2;
(3)根据V=
=
=
=250mL,
故答案为:250.
(2)根据N=
| m |
| M |
(3)根据V=
| n |
| C |
| ||
| C |
| ||
| 0.2mol/L |
故答案为:250.
点评:本题考查了物质的量的有关计算,根据物质的量的有关公式中各个物理量的关系来分析解答,熟记基本公式,灵活运用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )
| A、NaOH |
| B、SiO2 |
| C、Fe |
| D、H2O |
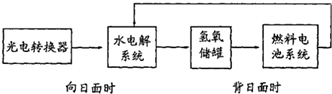 右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )
右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )| A、该能量转化系统工作时,需不断补充H2O |
| B、该转化系统的能量本质上来源于太阳能 |
| C、水电解系统中的阴极反应:4OH--4e-=O2+2H2O |
| D、燃料电池放电时的负极反应:H2-2e-=2H+ |
下列说法中正确的是( )
| A、化学性质相似的有机物一定是同系物 |
| B、分子组成相差一个或几个CH2原子团的有机物一定是同系物 |
| C、若烃中碳、氢元素的质量分数相同,它们必定是同系物 |
| D、互为同分异构体的两种有机物一定不能互称为同系物 |
硫在下列变化中,与分子间作用力有关的是( )
| A、硫蒸气的冷凝 |
| B、硫在氧气燃烧 |
| C、加热条件下硫与氢气反应 |
| D、加热条件下硫与铁反应 |
 根据反应:mA(g)+nB(g)?pC(g)△H,结合图中所给的信息填空.
根据反应:mA(g)+nB(g)?pC(g)△H,结合图中所给的信息填空.