题目内容
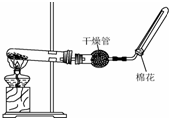
16.如图为某同学进行浓硫酸稀释的示意图,其中错误之处有( )
| A. | 1处 | B. | 2处 | C. | 3处 | D. | 4处 |
分析 瓶塞没有倒放;浓硫酸稀释是将浓硫酸倒入水中;没有用玻璃棒搅拌;标签没有对手心,据此解题.
解答 解:瓶塞没有倒放;浓硫酸稀释是将浓硫酸倒入水中;没有用玻璃棒搅拌;标签没有对手心,共4处错误.
故选D.
点评 本题考查物质的溶解与加热,难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
6.用CaSO4代替O2与燃料CO反应是一种高效、清洁的新型燃烧技术.反应如下:
①$\frac{1}{4}$CaSO4(s)+CO(g)?$\frac{1}{4}$CaS(s)+CO2(g)△H1=-47.3 kJ•mol-1
②CaSO4(s)+CO(g)?CaO(s)+CO2(g)+SO2(g)△H2=+210.5kJ•mol-1
③CO(g)?$\frac{1}{2}$C(s)+$\frac{1}{2}$CO2(g)△H3=-86.2kJ•mol-1.
下列说法错误的是( )
①$\frac{1}{4}$CaSO4(s)+CO(g)?$\frac{1}{4}$CaS(s)+CO2(g)△H1=-47.3 kJ•mol-1
②CaSO4(s)+CO(g)?CaO(s)+CO2(g)+SO2(g)△H2=+210.5kJ•mol-1
③CO(g)?$\frac{1}{2}$C(s)+$\frac{1}{2}$CO2(g)△H3=-86.2kJ•mol-1.
下列说法错误的是( )
| A. | 反应①达到平衡时,增大压强平衡不移动 | |
| B. | 反应②的平衡常数表达式为K=$\frac{c(C{O}_{2})•c(S{O}_{2})}{C(CO)}$ | |
| C. | 反应①和②是主反应,反应③是副反应 | |
| D. | 2CaSO4(s)+7CO(g)?CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)是放热反应 |
7.有机反应中常用镍作催化剂,某化工厂收集的镍催化剂中含Ni 64.0%,Al 24.3%、Fe 1.4%,其余为SiO2和有机物.这些含镍废催化剂经乙醇洗涤后可按下列工艺流程回收镍:

已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:
请回答下列问题:
(1)滤液A中存在的阴离子主要是AlO2-、SiO32-、OH-.
(2)硫酸浸取滤渣a后,所得滤液B中可能含有的金属离子是Fe2+、Ni2+.
(3)滤液B中加入H2O2的目的是将Fe2+氧化成Fe3+,有利于分离.操作X的名称是蒸发浓缩、冷却结晶.
(4)含镍金属氢化物MH-Ni燃料电池是一种绿色环保电池,广泛应用于电动汽车.其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液.它的充、放电反应为:xNi(OH)2+M$?_{放电}^{充电}$MHx+xNiOOH,电池充电过程中阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O,放电时负极的电极反应式为MHx+xOH--xe-=M++xH2O.

已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(1)滤液A中存在的阴离子主要是AlO2-、SiO32-、OH-.
(2)硫酸浸取滤渣a后,所得滤液B中可能含有的金属离子是Fe2+、Ni2+.
(3)滤液B中加入H2O2的目的是将Fe2+氧化成Fe3+,有利于分离.操作X的名称是蒸发浓缩、冷却结晶.
(4)含镍金属氢化物MH-Ni燃料电池是一种绿色环保电池,广泛应用于电动汽车.其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液.它的充、放电反应为:xNi(OH)2+M$?_{放电}^{充电}$MHx+xNiOOH,电池充电过程中阳极的电极反应式为Ni(OH)2+OH--e-=NiOOH+H2O,放电时负极的电极反应式为MHx+xOH--xe-=M++xH2O.
1.氢气在氯气中燃烧,会发出( )
| A. | 苍白色火焰 | B. | 淡黄色火焰 | C. | 蓝紫色火焰 | D. | 耀眼白光 |
8.下列物质所含的分子数(或原子数)等于阿伏加德罗常数的是( )
| A. | 0.5mo1 C2H4 | B. | 11.2L(标准状况) C2H2 气体 | ||
| C. | 23g Na | D. | 9g H2O |
5.如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许Na+通过.已知电池充、放反应的化学方程式为 2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr.当闭合开关K时,X极上有红色物质析出,下列说法正确的是( )
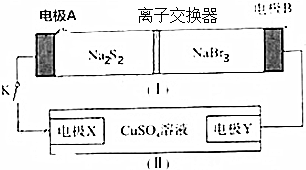

| A. | 装置①中钠离子从右到左通过离子交换膜 | |
| B. | B极的电极反应式为NaBr3+2e-+2Na═3NaBr | |
| C. | X电极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 每有0.1mol Na+通过离子交换膜,X电极上析出固体物质0.64g |
 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{+X}{→}$B$\stackrel{+X}{→}$C
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{+X}{→}$B$\stackrel{+X}{→}$C

 .
.
 (该物质易被氧化).请写出以
(该物质易被氧化).请写出以 、CH3COCl、CH3OH为原料制备
、CH3COCl、CH3OH为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C═CH2$\stackrel{Hr_{2}}{→}$
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C═CH2$\stackrel{Hr_{2}}{→}$