题目内容
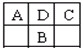 A、B、C、D为短周期元素,在周期表中如图所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法不正确的是( )
A、B、C、D为短周期元素,在周期表中如图所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法不正确的是( )| A、A的氧化物有多种形式 |
| B、B的最高价氧化物对应的水化物是一种强酸 |
| C、D元素形成的单质不止一种 |
| D、C的氢化物水溶液通常用玻璃试剂瓶盛放 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为短周期元素,根据元素在周期表中的位置知,A、D、C是第二周期元素,B是第三周期元素,A、C两种元素的原子核外电子数之和等于B原子的核电荷数,设A的原子序数是a,则C的原子序数是a+2,B的原子序数是a+9,a+a+2=a+9,所以a=7,则A是N元素、B是S元素、C是F有、D是O元素,再结合元素周期律及物质的性质解答.
解答:
解:A、B、C、D为短周期元素,根据元素在周期表中的位置知,A、D、C是第二周期元素,B是第三周期元素,A、C两种元素的原子核外电子数之和等于B原子的核电荷数,设A的原子序数是a,则C的原子序数是a+2,B的原子序数是a+9,a+a+2=a+9,所以a=7,则A是N元素、B是S元素、C是F有、D是O元素,
A.A是N元素,N元素的氧化物有NO、N2O、N2O5等,故A正确;
B.B是S元素,S元素的最高价氧化物的水化物是硫酸,硫酸是强酸,故B正确;
C.D元素是O元素,其单质有氧气、臭氧,故C正确;
D.C的氢化物是HF,玻璃的主要成分是二氧化硅,HF能和二氧化硅发生反应4HF+SiO2=SiF4+2H2O,所以不能用玻璃棒盛放,故D错误;
故选D.
A.A是N元素,N元素的氧化物有NO、N2O、N2O5等,故A正确;
B.B是S元素,S元素的最高价氧化物的水化物是硫酸,硫酸是强酸,故B正确;
C.D元素是O元素,其单质有氧气、臭氧,故C正确;
D.C的氢化物是HF,玻璃的主要成分是二氧化硅,HF能和二氧化硅发生反应4HF+SiO2=SiF4+2H2O,所以不能用玻璃棒盛放,故D错误;
故选D.
点评:本题考查了元素周期表和元素周期律的综合应用,根据元素位置确定元素,再结合物质的性质、基本概念、元素周期律等知识点来分析解答,题目难度不大,易错选项是D.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )
| A、铊是易导电的银白色金属 |
| B、Tl(OH)3是两性氢氧化物 |
| C、能生成+3价离子化合物 |
| D、Tl3+的氧化能力比Al3+强 |
已知X、Y、Z、W是原子序数依次增大的短周期元素,这些元素的其他信息如下表.下列说法正确的是( )
| 元素 | 信息 |
| X | K层电子数是L层电子数的2倍 |
| Y | 一种核素在考古时常用来鉴定一些文物的年代 |
| Z | 所处的周期序数与族序数相等 |
| W | 最高价氧化物对应的水化物酸性最强 |
| A、W的阴离子半径大于Z的阳离子半径 |
| B、Y的氢化物比W的氢化物稳定 |
| C、Z的最高价氧化物对应的水化物不能够溶于Y的最高价氧化物对应的水化物 |
| D、X在氧气中加热反应生成X2O2 |
某混和气体可能含有H2、CO、CO2、HCl、NH3和水蒸气中的两种或多种,当混和气体依次通过:①澄清石灰水(无浑浊现象);②氢氧化钡溶液(有浑浊现象);③浓H2SO4(无现象);④灼热氧化铜(变红);⑤无水硫酸铜(变蓝).(假设每一次吸收均完全).对该混和气体成分判断正确的是( )
| A、一定没有CO2,肯定有H2 |
| B、一定有CO、CO2和水蒸气? |
| C、一定有H2、CO2和HCl |
| D、可能有CO2、NH3和水蒸气? |
警察常从案发现场的人体气味来获取有用的线索,人体气味的成分中含有多种有机物,比如:
①十八烷
②环十二醇,
关于这二种有机物,下列说法不正确的是( )
①十八烷
②环十二醇,
关于这二种有机物,下列说法不正确的是( )
| A、①和②分子中碳原子数大于10 |
| B、①和②常温常压下不为气态 |
| C、①和②均能与Na反应放出氢气 |
| D、②的分子式为C12H24O |
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( )
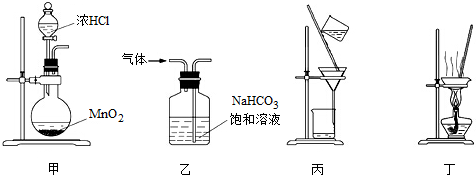

| A、用装置甲制取氯气 |
| B、用装置乙除去氯气中混有的少量氯化氢 |
| C、用装置丙分离二氧化锰和氯化锰溶液 |
| D、用装置丁蒸干氯化锰溶液制MnCl2?4H2O |
 实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
实验室需要配制0.50mol/L NaCl溶液480mL.按下列操作步骤填上适当的文字,以使整个操作完整.
 化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题;
化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题;