题目内容
下列说法,正确的是( )
①活化分子间的碰撞一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③活化分子比普通分子具有较高的能量
④化学反应的实质是原子的重新组合
⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程
⑥化学反应的实质是活化分子有合适取向时的有效碰撞.
①活化分子间的碰撞一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③活化分子比普通分子具有较高的能量
④化学反应的实质是原子的重新组合
⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程
⑥化学反应的实质是活化分子有合适取向时的有效碰撞.
| A、②③⑥ | B、③④⑤ |
| C、②④⑤ | D、①③④⑤ |
考点:化学反应速率的影响因素,反应热和焓变
专题:化学反应中的能量变化,化学反应速率专题
分析:①活化分子间的碰撞不一定为有效碰撞;
②普通分子间的碰撞,达不到反应所需的能量;
③活化分子具有较高的能量;
④化学变化中的最小微粒为原子;
⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程;
⑥化学反应的实质与化学键有关.
②普通分子间的碰撞,达不到反应所需的能量;
③活化分子具有较高的能量;
④化学变化中的最小微粒为原子;
⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程;
⑥化学反应的实质与化学键有关.
解答:
解:①活化分子间的碰撞不一定为有效碰撞,则不一定发生化学反应,故错误;
②普通分子间的碰撞,达不到反应所需的能量,则不能发生化学反应,故错误;
③活化分子具有较高的能量,可发生反应,而普通分子不具有反应所需的能量,故正确;
④化学变化中的最小微粒为原子,则化学反应的实质是原子的重新组合,故正确;
⑤从化学键角度可知,化学反应的实质是旧化学键的断裂和新化学键的形成过程,故正确;
⑥化学反应的实质与化学键有关,活化分子有合适取向时的有效碰撞一定发生化学反应,为化学反应的前提,故错误;
故选B.
②普通分子间的碰撞,达不到反应所需的能量,则不能发生化学反应,故错误;
③活化分子具有较高的能量,可发生反应,而普通分子不具有反应所需的能量,故正确;
④化学变化中的最小微粒为原子,则化学反应的实质是原子的重新组合,故正确;
⑤从化学键角度可知,化学反应的实质是旧化学键的断裂和新化学键的形成过程,故正确;
⑥化学反应的实质与化学键有关,活化分子有合适取向时的有效碰撞一定发生化学反应,为化学反应的前提,故错误;
故选B.
点评:本题考查活化分子及化学反应的关系,为高频考点,把握活化理论为解答的关键,侧重分析与理解应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分子式为C5H12O并能与金属钠反应放出氢气的有机化合物有( )
| A、6种 | B、7种 | C、8种 | D、9种 |
下列关于热化学反应的描述中正确的是( )
A、葡萄糖的燃烧热是2800 kJ?mol-1,则
| ||
B、燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+
则CH3OH(g)的燃烧热为192.9 kJ?mol-1 | ||
| C、H2(g)的燃烧热是285.8 kJ?mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 | ||
| D、已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ?mol-1 |
下列离子反应方程书写正确的是( )
| A、H2O+H2O?H3O++OH- |
| B、CO32-+2H2O?H2CO3+2OH- |
| C、Ca(OH)2+2H+?Ca2++2H2O |
| D、Al3++3H2O═Al(OH)3↓+3H+ |
有芳香气味的C9H18O2在酸性条件下加热可水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有( )
| A、8种 | B、14种 |
| C、16种 | D、18种 |
已知三种一元弱酸的酸性强弱 :HX>HY>HZ,则相同物质的量浓度的这三种酸的钠盐溶液pH由大到小的顺序正确的是( )
| A、NaX、NaY、NaZ |
| B、NaZ、NaY、NaX |
| C、NaY、NaZ、NaX |
| D、NaX、NaZ、NaX |
下列离子方程式正确的是( )
| A、用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O | ||||
| B、小苏打溶液中加足量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | ||||
C、用石墨作电极电解饱和NaCl溶液:2Cl-+2H2O
| ||||
| D、向氯化铝溶液中通入过量的氨气:Al3++4OH-═AlO2-+2H2O |
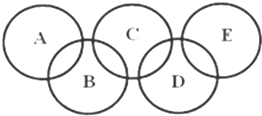 如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为
如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C、D均为原子晶体,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: