题目内容
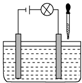 在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )
在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )| A、盐酸中逐滴加入食盐溶液 |
| B、醋酸中逐滴加入氢氧化钠溶液 |
| C、饱和石灰水中不断通入CO2 |
| D、醋酸中逐滴加入氨水 |
考点:电解质溶液的导电性
专题:电离平衡与溶液的pH专题
分析:若向某一电解质溶液中逐滴加入另一溶液时,灯泡由亮变暗,说明溶液中电解质的浓度降低,说明所加入物质能与溶液中电解质反应生成弱电解质或沉淀,至熄灭后又逐渐变亮,说明完全反应时溶液电荷浓度接近0,当另一溶液过量时,溶液中电荷浓度逐渐增大,又逐渐变亮,以此解答.
解答:
解:A.食盐溶液中逐滴加入盐酸,溶液电荷浓度不为0,灯泡不可能熄灭,故A错误;
B.醋酸中逐滴加入氢氧化钠溶液生成醋酸钠,溶液电荷浓度不为0,灯泡不可能熄灭,故B错误;
C.饱和石灰水中不断通入CO2,完全反应时生成碳酸钙和水,溶液电荷浓度接近0,灯泡熄灭,符合题目要求,故C正确;
D.醋酸中逐滴加入氨水,生成醋酸铵,溶液电荷浓度不为0,灯泡不可能熄灭,故D错误.
故选C.
B.醋酸中逐滴加入氢氧化钠溶液生成醋酸钠,溶液电荷浓度不为0,灯泡不可能熄灭,故B错误;
C.饱和石灰水中不断通入CO2,完全反应时生成碳酸钙和水,溶液电荷浓度接近0,灯泡熄灭,符合题目要求,故C正确;
D.醋酸中逐滴加入氨水,生成醋酸铵,溶液电荷浓度不为0,灯泡不可能熄灭,故D错误.
故选C.
点评:本题考查电解质溶液的导电性,题目难度不大,注意灯泡熄灭,说明完全反应时溶液电荷浓度接近0,根据反应物进行判断.

练习册系列答案
相关题目
下列说法正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(g),△H=-483.6kJ?mol-1,则H2的燃烧热为-241.8kJ?mol-1 | ||||||||||
B、已知:25℃时,
| ||||||||||
C、反应Fe(s)+5CO(g)?Fe(CO)5(g)的平衡常数表达式为K=
| ||||||||||
D、0.1mol?L-1的酒石酸(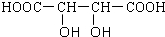 )与0.1mol?L-1的NaOH混合后:c(HC4H4O6-)+2c(C4H4O62-)=c(Na+)+c(H+)-c(OH-) )与0.1mol?L-1的NaOH混合后:c(HC4H4O6-)+2c(C4H4O62-)=c(Na+)+c(H+)-c(OH-) | ||||||||||
在甲、乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、CO32-、Cl-、OH- 六中离子中的三种,已知乙烧杯中的溶液呈碱性,则甲烧杯中可能含有的离子是( )
| A、Cu2+、H+、Cl- |
| B、CO32-、OH- Cl- |
| C、K+、H+、Cl- |
| D、K+、CO32-、OH- |
下列说法正确的是( )
| A、用玻璃棒蘸取待测样品溶液于无色火焰上灼烧,焰色为黄色,说明样品含钠元素 |
| B、将移液管中液体放出时,移液管不能与容器内壁接触,以免污染试剂 |
| C、可以用蒸馏水润湿的pH试纸检验氨气 |
| D、检验红色砖块中是否含三价铁的步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |
下列化学用语正确的是( )
| A、乙醇的结构简式:C2H6O | ||||
B、CH4的比例模型: | ||||
C、工业上制取粗硅的化学方程式:SiO2+C
| ||||
| D、电解饱和食盐水的离子方程式:Cl-+2H2O═Cl2↑+2OH-+H2↑ |
既能发生消去反应生成烯,又能发生催化氧化生成醛的是( )
| A、甲醇 |
| B、苯甲醇 |
| C、2-甲基-1-丙醇 |
| D、2-甲基-2-丙醇 |



