题目内容
4.在CH3COOH溶液中存在:CH3COOH?CH3COO-+H+常温下加水稀释,下列分析正确的是( )| A. | c(OH-)减小 | B. | c(CH3COO-) 增大 | ||
| C. | pH减小 | D. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大 |
分析 在CH3COOH溶液中存在:CH3COOH?CH3COO-+H+常温下加水稀释,促进电离,但溶液的体积变大,由此分析解答.
解答 解:A、CH3COOH?CH3COO-+H+常温下加水稀释,促进电离,但溶液体积变大,氢离子浓度减小,根据水的离子积氢离子和氢氧根离子的浓度之积是一个定值,所以c(OH-)增大,故A错误;
B、CH3COOH?CH3COO-+H+常温下加水稀释,促进电离,但溶液体积变大,c(CH3COO-)减小,故B错误;
C、CH3COOH?CH3COO-+H+常温下加水稀释,促进电离,但溶液体积变大,氢离子浓度减小,PH值增大,故C错误;
D、$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$=$\frac{{K}_{a}}{c(C{H}_{3}CO{O}^{-})}$,CH3COOH?CH3COO-+H+常温下加水稀释,促进电离,但溶液体积变大,c(CH3COO-)减小,所以$\frac{{K}_{a}}{c(C{H}_{3}CO{O}^{-})}$增大,故D正确;
故选D.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点及影响弱电解质电离的因素即可解答,注意D通过转变判断浓度之比变化,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
14.三瓶无色溶液,分别为NH4Cl、Na2CO3、NaOH;只用一种试剂一次区分开,该试剂是( )
| A. | AgNO3溶液 | B. | 稀硫酸 | C. | 酚酞 | D. | Ba(OH)2溶液 |
15.现有MgCl2和Al2(SO4)3混合溶液,向其中不断加入Na2O2,得到沉淀的量与加入Na2O2的物质的量如图所示,原溶液中Cl-与SO42-的物质的量之比为( )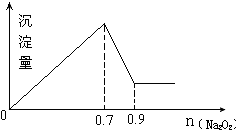

| A. | 1:3 | B. | 2:3 | C. | 6:1 | D. | 3:1 |
12.分子式为C5H10O2并能饱和NaHCO3,溶液反应放出气体的有机物有(不含立体结构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
19.将8g铁片放入100mL硫酸铜溶液中,溶液中的Cu2+全部被还原时,铁片变为8.2g,则原c(CuSO4)为( )
| A. | 0.25 mol•L-1 | B. | 0.025 mol•L-1 | C. | 0.5 mol•L-1 | D. | 0.125 mol•L-1 |
13.化学工业是国民经济的支柱产业,下列生产过程中不涉及化学变化的是( )
| A. | 氮肥厂用氢气和氮气合成氨 | |
| B. | 钢铁在潮湿空气中生锈 | |
| C. | 往硫酸铜晶体上滴入浓硫酸,颜色由蓝色变成白色 | |
| D. | 石油分馏后得汽油、煤油等 |
10.固体X中可能含有MgCl2、Na2CO3、K2SO3、KAlO2中的一种或几种.为确定该固体粉末的成分,现取X进行下列实验,实验过程及现象如下

根据上述实验,下列说法正确的是( )

根据上述实验,下列说法正确的是( )
| A. | 气体1可能为NO和CO2的混合物 | |
| B. | 沉淀3可能为Mg(OH)2和Al(OH)3的混合物 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | 固体粉末X中一定有Na2CO3,可能有KAlO2 |
