题目内容
9.海水中含有大量的氯化镁,从海水中提取镁的生产流程如图所示:
试回答下列问题:
(1)操作①的名称是过滤.操作②包括一系列操作:依次为蒸发浓缩、冷却结晶、过滤.
(2)加入试剂①时所发生反应的离子方程式为Mg(OH)2+2H+═Mg2++2H2O.
(3)如果生成的Mg(OH)2中含有少量Ca(OH)2,可选用MgCl2溶液加入除去.
分析 从海水中提取金属镁的流程:把贝壳制成石灰乳操作①,在引入的海水中加入石灰乳,将海水中含有的镁离子转化为氢氧化镁沉淀,反应方程式为:Mg2++2OH-=Mg(OH)2↓,然后将氢氧化镁溶于盐酸中操作②得到氯化镁溶液,反应方程式为:Mg(OH)2+2HCl=MgCl2+2H2O,用氯化镁溶液在氯化氢氛围中制取无水氯化镁,活泼金属采用电解其熔融盐的方法冶炼,镁是活泼金属,最后利用电解熔融氯化镁的方法冶炼镁操作③,反应方程式为MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(1)在海水中加入氧化钙,氧化钙和水反应生成氢氧化钙,氢氧化钙和海水中的氯化镁发生复分解反应生成氢氧化镁;从液体中得到沉淀氢氧化镁用过滤的方法分离,从溶液中析出固体采用蒸发结晶的方法得到;
(2)利用盐酸溶解氢氧化镁不引入其它杂质离子;
(3)生成的Mg(OH)2中含有少量Ca(OH)2,可以利用氢氧化镁溶解性小,加入氯化镁溶液洗涤过滤除去;
解答 解:(1)在海水中加入氧化钙发生反应:CaO+H2O═Ca(OH)2;氢氧化钙和海水中的氯化镁发生复分解反应:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2,氢氧化镁是难溶性的固体,将不溶性的固体和溶液分离的方法是过滤,所以操作①主要是指过滤,操作②是从溶液中析出固体,采用蒸发浓缩,冷却结晶,过滤洗涤的方法得到MgCl2•6H2O,
故答案为:过滤,蒸发浓缩、冷却结晶;
(2)加入试剂①时所发生反应是将氢氧化镁溶于盐酸中得到氯化镁溶液,不引入其它杂质阴离子,所以试剂①为盐酸,反应的离子方程式为:Mg(OH)2+2H+═Mg2++2H2O,
故答案为:Mg(OH)2+2H+═Mg2++2H2O;
(3)如果生成的Mg(OH)2中含有少量Ca(OH)2,加入氯化镁溶液,Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2,过滤得到氢氧化镁沉淀,除去氢氧化钙,
故答案为:MgCl2溶液;
点评 本题考查了镁的提取,掌握从海水中提取金属镁的流程:先将海水中含有的镁离子转化为氢氧化镁沉淀,然后将氢氧化镁溶于盐酸中得到氯化镁溶液,用氯化镁溶液制取无水氯化镁,最后利用电解熔融氯化镁的方法冶炼镁,是解答的关键,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | M只能是碱类 | B. | M只能是盐类 | C. | M一定为电解质 | D. | M可能为非电解质 |
| A. | c(OH-)减小 | B. | c(CH3COO-) 增大 | ||
| C. | pH减小 | D. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大 |
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A. | 在冰醋酸中,高氯酸的酸性最强 | |
| B. | 水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱 | |
| C. | 在冰醋酸中1mol/L的高氯酸的电离度约为0.4% | |
| D. | 在冰醋酸中硫酸的电离方程式为:H2SO4═2H++SO42- |
| A. | 2A+3B═2C | B. | A+3B═2C | C. | 3A+B═2C | D. | 3A+2B═3C |
| A. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸在常温下不容易与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 浓硫酸在常温下能够使铁、铝、锌等金属钝化 |
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.8 | 6.3 | 5.2 |
| 完全沉淀的pH | 3.0 | 8.3 | 6.7 |
实验步骤:
Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,过滤得固体A和无色溶液B;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微热,固体完全溶解,得溶液C;
Ⅳ.向C中加入NaClO,调节溶液的pH至4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D;
Ⅴ.向D中加入NaOH,调节溶液的pH到7~8,产生蓝色絮状沉淀. 请回答下列问题.
(1)Ⅰ中产生气体的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.
(2)由Ⅰ、Ⅱ知,原样品中一定不存在的物质是SiO2.
(3)溶液C中除H+、Cu2+外一定还含有的阳离子是Fe2+;为验证溶液C中存在该阳离子,可选用的试剂及对应的现象是向酸性KMnO4溶液中滴加待测液,褪色.
(4)Ⅳ中加NaClO的目的是将Fe2+氧化成Fe3+,增大溶液的pH使Fe3+生成Fe(OH)3沉淀.
(5)由上述实验可以获得结论:原样品所有可能的成分组合为组合1:Al、Fe2O3、Cu2O;组合2:Al、Cu2O、Fe3O4(Al、Fe2O3、Cu2O、Fe3O4); …(用化学式表示,空不够可以补充.)
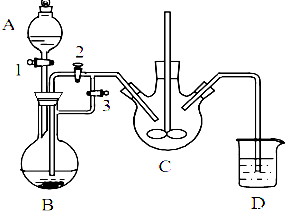 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得: