题目内容
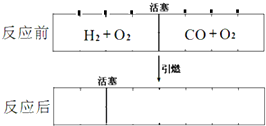 在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器.左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体.同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)
在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器.左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体.同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)①1:1 ②3:1 ③1:3 ④1:2( )
| A、①② | B、②④ | C、①④ | D、①③ |
考点:化学方程式的有关计算
专题:计算题
分析:假设氢气和氧气的物质的量分别为1mol,开始时左右两侧气体的体积相等,则物质的量之和相等,右侧气体共为2mol,根据方程式计算左室中剩余气体物质的量,由图可知反应后左右两侧气体的物质的量之比为1:3,讨论右侧剩余气体,根据反应的有关方程式判断.
解答:
解:假设氢气和氧气的物质的量分别为1mol,开始时左右两侧气体的体积相等,则物质的量之和相等,右侧气体共为2mol,同时引燃左右两侧的混合气,
左侧:2H2+O2
2H2O,
1mol 0.5mol
左侧剩余气体为0.5molO2,由图可知反应后左右两侧气体的体积之比为2:6=1:3,故物质的量之比为1:3,则右侧气体的物质的量为0.5mol×3=1.5mol,
当CO过量时,设O2为xmol,则CO为(2-x)mol:
2CO+O2
2CO2
2 1 1
2x x 2x
2-x-2x+2x=1.5,解得x=0.5
所以n(CO)=2mol-0.5mol=1.5mol,则n(CO):n(O2)=3:1;
当O2过量时,设CO为ymol,则O2为(2-y)mol,
2CO+O2
2CO2
2 1 1
y
y
2-y-
+y=1.5
解得y=1,
所以,n(CO)=1mol,n(O2)=1mol,则n(CO):n(O2)=1:1,
故选A.
左侧:2H2+O2
| ||
1mol 0.5mol
左侧剩余气体为0.5molO2,由图可知反应后左右两侧气体的体积之比为2:6=1:3,故物质的量之比为1:3,则右侧气体的物质的量为0.5mol×3=1.5mol,
当CO过量时,设O2为xmol,则CO为(2-x)mol:
2CO+O2
| ||
2 1 1
2x x 2x
2-x-2x+2x=1.5,解得x=0.5
所以n(CO)=2mol-0.5mol=1.5mol,则n(CO):n(O2)=3:1;
当O2过量时,设CO为ymol,则O2为(2-y)mol,
2CO+O2
| ||
2 1 1
y
| y |
| 2 |
2-y-
| y |
| 2 |
解得y=1,
所以,n(CO)=1mol,n(O2)=1mol,则n(CO):n(O2)=1:1,
故选A.
点评:本题考查化学方程式的计算,题目难度中等,注意根据左右两侧气体的体积关系判断右侧气体的物质的量,用讨论的方法计算.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列有关物质鉴别或检验的说法不正确的是( )
| A、利用酸性高锰酸钾溶液鉴别SO2和CO2 |
| B、利用氢氧化钡溶液鉴别氯化铵和硫酸铵 |
| C、可以用KSCN溶液检验FeSO4固体是否变质 |
| D、用干燥的有色布条检验氯化氢气体中是否含有氯气 |
下列说法中,不正确的是( )
| A、双原子分子中的共价键,一定是极性键 |
| B、非极性键也可能存在于离子化合物中 |
| C、物理变化可能破坏化学键 |
| D、离子化合物在固态时不能导电 |
下列有关金属及化合物的说法正确的是( )
| A、地壳中含量最多的元素是铝元素 |
| B、在自然界中铝以化合态存在 |
| C、NaCl的焰色反应呈紫色 |
| D、白色絮状沉淀Fe(OH)2可溶于NaOH溶液中 |
配制一定体积、一定物质的量浓度的溶液时,下列会使配得的溶液浓度偏低的是( )
| A、容量瓶中原有少量蒸馏水 |
| B、溶液从烧杯转移到容量瓶中后没有洗涤烧杯和玻璃棒 |
| C、定容时观察液面俯视 |
| D、定容时平视液面 |
下列说法正确的是( )
| A、2-丁烯不存在顺反异构体 |
| B、已知丙烷的二氯代物有四种异构体,则其六氯代物的异构体数目为六种 |
C、菲的结构简式为  ,它与硝酸反应,可生成4种一硝基取代物 ,它与硝酸反应,可生成4种一硝基取代物 |
| D、乙醛的核磁共振氢谱中有二个峰,峰面积之比是1:3 |