题目内容
下列说法中,不正确的是( )
| A、双原子分子中的共价键,一定是极性键 |
| B、非极性键也可能存在于离子化合物中 |
| C、物理变化可能破坏化学键 |
| D、离子化合物在固态时不能导电 |
考点:极性键和非极性键,离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:A、根据两原子是否为同一元素的原子分析;
B、过氧化钠属于离子化合物,其中含有非极性键;
C、氯化氢溶于水,破坏了共价键;
D、离子化合物处于固态时,阴阳离子之间受到离子键的作用,不能自由移动.
B、过氧化钠属于离子化合物,其中含有非极性键;
C、氯化氢溶于水,破坏了共价键;
D、离子化合物处于固态时,阴阳离子之间受到离子键的作用,不能自由移动.
解答:
解:A、双原子分子中的共价键,若为同一元素的原子形成的,一定为非极性键,若为两种不同的元素的原子形成的,一定为极性键,故A错误;
B、过氧化钠属于离子化合物,过氧根离子中O与O形成的化学键为非极性键,故B正确;
C、氯化氢溶于水电离得到自由移动的氢离子和氯离子,破坏了共价键,故C正确;
D、离子化合物处于固态时,阴阳离子之间受到离子键的作用,不能自由移动,因此不能导电,故D正确;
故选A.
B、过氧化钠属于离子化合物,过氧根离子中O与O形成的化学键为非极性键,故B正确;
C、氯化氢溶于水电离得到自由移动的氢离子和氯离子,破坏了共价键,故C正确;
D、离子化合物处于固态时,阴阳离子之间受到离子键的作用,不能自由移动,因此不能导电,故D正确;
故选A.
点评:本题考查了共价键的类型、离子化合物的特征与性质,深刻理解极性键、非极性键、离子化合物的定义,结合已学物质进行即可解答.

练习册系列答案
 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
下列各组指定物质的同分异构体数目相等的是( )
| A、乙烷的二氯代物和丙烷的一氯代物 |
| B、丙烷的一氯代物和戊烷 |
| C、苯的二氯代物和苯的一硝基代物 |
| D、C3H6和C5H12 |
下列有关有机物的说法错误的是( )
| A、酸性KMnO4溶液既可以用于鉴别CH4与CH2=CH2,又可以用于除去CH4中混有的CH2=CH2 |
| B、乙醇、乙酸和乙酸乙酯均能发生取代反应 |
| C、苯、甲苯互为同系物,都能发生氧化反应和加成反应 |
| D、在苯酚溶液中,滴入少量稀溴水,不会立即产生白色沉淀 |
元素周期表中位置相近的元素性质相似,人们可以借助元素周期表研究合成有特定性质的新物质.为合成具有半导体性质的材料,适宜在周期表中哪个区域寻找( )
| A、金属与非金属交界处 |
| B、过渡元素区域(副族和第Ⅷ族) |
| C、长周期金属元素区域 |
| D、长周期非金属元素区域 |
对人体健康不会造成危害的是( )
| A、用工业酒精(含甲醇)兑制饮用酒 |
| B、用食醋除去水壶内壁的水垢 |
| C、用甲醛水溶液浸泡海产品进行防腐保鲜 |
| D、在不通风、无防护的条件下用苯做实验 |
下列装置烧杯中盛放的都是稀硫酸,在铜上能产生大量气泡的是( )
A、 |
B、 |
C、 |
D、 |
下列有机物中,常温常压下呈气态的是( )
| A、己烯 | B、硝基苯 |
| C、甘油 | D、一氯甲烷 |
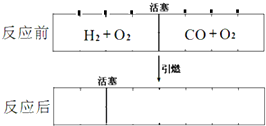 在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器.左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体.同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)
在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器.左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体.同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)