题目内容
下列实验操作不能达到预期的目的是( )
| 实验目的 | 操作 | |
| A | 证明CH2=CHCH2OH中含有碳碳双键 | 滴入溴水 |
| B | 欲证明浓硫酸有脱水性和强氧化性 | 将浓硫酸滴到蔗糖上 |
| C | 证明FeCl2溶液中含有Fe2+ | 加入酸性KMnO4溶液 |
| D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.碳碳双键与溴水发生加成反应,-OH不反应;
B.浓硫酸使蔗糖变黑,为脱水性;C与浓硫酸反应为强氧化性;
C.亚铁离子、氯离子,在酸性条件下均能被高锰酸钾氧化;
D.石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,铜离子先放电.
B.浓硫酸使蔗糖变黑,为脱水性;C与浓硫酸反应为强氧化性;
C.亚铁离子、氯离子,在酸性条件下均能被高锰酸钾氧化;
D.石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,铜离子先放电.
解答:
解:A.碳碳双键与溴水发生加成反应,-OH不反应,则滴入溴水可检验碳碳双键,故A正确;
B.浓硫酸使蔗糖变黑,为脱水性;C与浓硫酸反应生成二氧化硫,体现其强氧化性,则操作与目的均合理,故B正确;
C.亚铁离子、氯离子,在酸性条件下均能被高锰酸钾氧化,则不能确定是否含Fe2+,故C错误;
D.石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,铜离子先放电,氧化性铜离子大于镁离子,则金属性Mg>Cu,故D正确;
故选C.
B.浓硫酸使蔗糖变黑,为脱水性;C与浓硫酸反应生成二氧化硫,体现其强氧化性,则操作与目的均合理,故B正确;
C.亚铁离子、氯离子,在酸性条件下均能被高锰酸钾氧化,则不能确定是否含Fe2+,故C错误;
D.石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液,铜离子先放电,氧化性铜离子大于镁离子,则金属性Mg>Cu,故D正确;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及离子的检验、官能团的检验、氧化还原反应及电解原理等,把握化学反应原理及物质性质为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
下列实验操作或装置(略去部分夹持仪器)正确的是( )
A、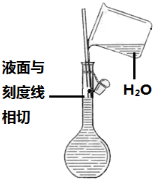 配制溶液 |
B、 中和滴定 |
C、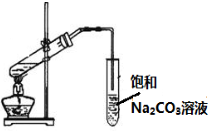 制备乙酸乙醇 |
D、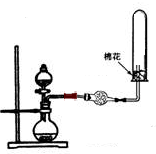 制备收集干燥的氨气 |
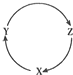 下列各组物质中,不能满足如图一步转化关系的选项是( )
下列各组物质中,不能满足如图一步转化关系的选项是( )| 编号 | X | Y | Z |
| ① | Mg | MgO | MgCl2 |
| ② | H2SO4 | SO2 | SO3 |
| ③ | SiO2 | H2SiO3 | Na2SiO3 |
| ④ | Na | NaOH | NaHCO3 |
| ⑤ | Cu | CuSO4 | Cu(OH)2 |
| ⑥ | C | CO | CO2 |
| ⑦ | Cl2 | HCl | HClO |
| ⑧ | N2 | NH3 | NO |
| A、①②⑥⑦ | B、①③④⑦⑧ |
| C、③④⑤ | D、③④⑤⑥⑦ |
下列有关有机物的说法错误的是( )
| A、酸性KMnO4溶液既可以用于鉴别CH4与CH2=CH2,又可以用于除去CH4中混有的CH2=CH2 |
| B、乙醇、乙酸和乙酸乙酯均能发生取代反应 |
| C、苯、甲苯互为同系物,都能发生氧化反应和加成反应 |
| D、在苯酚溶液中,滴入少量稀溴水,不会立即产生白色沉淀 |
下列物质的化学式和结构式中,从成键情况看不合理的是( )
A、CH3N: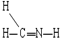 |
B、CH4S: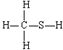 |
C、CH2SeO: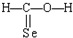 |
D、CH4Si: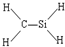 |
元素周期表中位置相近的元素性质相似,人们可以借助元素周期表研究合成有特定性质的新物质.为合成具有半导体性质的材料,适宜在周期表中哪个区域寻找( )
| A、金属与非金属交界处 |
| B、过渡元素区域(副族和第Ⅷ族) |
| C、长周期金属元素区域 |
| D、长周期非金属元素区域 |
对人体健康不会造成危害的是( )
| A、用工业酒精(含甲醇)兑制饮用酒 |
| B、用食醋除去水壶内壁的水垢 |
| C、用甲醛水溶液浸泡海产品进行防腐保鲜 |
| D、在不通风、无防护的条件下用苯做实验 |
根据原子结构及元素周期律的知识,下列推断正确的是( )
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 | ||||
| B、核外电子排布相同的微粒化学性质也相同 | ||||
| C、Cl-、S2-、Ca2+、K+半径逐渐减小 | ||||
D、
|
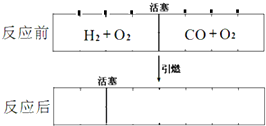 在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器.左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体.同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)
在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器.左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体.同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)