题目内容
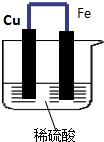
 利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个原电池(正极材料用碳棒).装置图
利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个原电池(正极材料用碳棒).装置图回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子1mol,则生成银
考点:设计原电池
专题:电化学专题
分析:在Cu+2Ag+=2Ag+Cu2+反应中,Cu被氧化,应为原电池的负极,电解反应为:Cu-2e-=Cu2+,Ag+得电子被还原生成单质Ag,正极上有银白色物质生成,电极反应为Ag++e-=Ag,应为原电池正极反应,正极材料为活泼性比Cu的金属或非金属材料,电解质溶液为含Ag+离子的溶液,如AgNO3,原电池工作时,电子从负极经外电路流向正极,溶液中阳离子向正极移动,阴离子向负极移动,以形成闭合回路.
解答:
解:选铜、C作电极材料,硝酸银溶液作电解质溶液,该装置图为 ,故答案为:
,故答案为: ;
;
(1)在Cu+2Ag+=2Ag+Cu2+反应中,Cu被氧化,应为原电池的负极,电解反应为:Cu-2e-=Cu2+,电解质溶液为含Ag+离子的溶液,如AgNO3,
故答案为:Cu;氧化;Cu-2e-=Cu2+;AgNO3溶液;
(2)Ag+得电子被还原生成单质Ag,正极上有银白色物质生成,电极反应为Ag++e-=Ag,应为原电池正极反应,
故答案为:碳棒上出现银白色物质;
(3)正极反应为Ag++e-=Ag,若导线上转移电子1mol,则生成银1mol,质量为108g,故答案为:108.
 ,故答案为:
,故答案为: ;
;(1)在Cu+2Ag+=2Ag+Cu2+反应中,Cu被氧化,应为原电池的负极,电解反应为:Cu-2e-=Cu2+,电解质溶液为含Ag+离子的溶液,如AgNO3,
故答案为:Cu;氧化;Cu-2e-=Cu2+;AgNO3溶液;
(2)Ag+得电子被还原生成单质Ag,正极上有银白色物质生成,电极反应为Ag++e-=Ag,应为原电池正极反应,
故答案为:碳棒上出现银白色物质;
(3)正极反应为Ag++e-=Ag,若导线上转移电子1mol,则生成银1mol,质量为108g,故答案为:108.
点评:本题考查原电池的设计,题目难度不大,把握两极材料的判断以及电极反应式的书写方法为解答的关键,注意设计原电池中信息中已知正极为C,而不能写成Ag等.

练习册系列答案
相关题目
在反应2KMnO4=K2MnO4+MnO2+O2↑中,氧化产物是( )
| A、K2MnO4 |
| B、MnO2 |
| C、O2 |
| D、KMnO4 |
下列离子方程式中正确的是( )
| A、氨水吸收过量的SO2:OH-+SO2=HSO3- |
| B、用氢氧化钠溶液除去镁粉中的铝粉:2Al+2OH-=AlO2-+H2↑ |
| C、KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+=I2+2H2O |
| D、碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO
)=0.2mol/L,当加入等体积、某浓度的KOH溶液时,恰好沉淀完全,则所得溶液中K+的物质的量浓度是( )
2- 4 |
| A、0.2 mol/L |
| B、0.25 mol/L |
| C、0.1 mol/L |
| D、0.225 mol/L |