题目内容
如图所示,将铁、铜通过导线相连,置于稀硫酸中.铁片为 极,电极上发生的是 反应(填“氧化”或“还原”),电极反应式为 ,铁片上观察到的现象为 .铜片为 极,电极上发生的是 反应,电极反应式是 ,铜片上观察到的现象是 .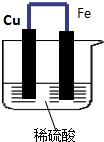

考点:原电池和电解池的工作原理
专题:电化学专题
分析:该原电池中,Fe易失电子作负极、Cu作正极,负极上电极反应式为Fe-2e-=Fe2+,正极上电极反应式为2H++2e-=H2↑,导致负极上金属逐渐减少,正极上有气泡产生.
解答:
解:该原电池中,Fe易失电子作负极、Cu作正极,负极上铁失电子发生氧化反应生成亚铁离子进入溶液,电极反应式为Fe-2e-=Fe2+,则负极上金属铁不断溶解,正极上氢离子得电子发生还原反应生成氢气,电极反应式为2H++2e-=H2↑,则正极上有气泡产生,
故答案为:负;氧化;Fe-2e-=Fe2+;铁片不断溶解;正;还原;2H++2e-=H2↑;有气泡产生.
故答案为:负;氧化;Fe-2e-=Fe2+;铁片不断溶解;正;还原;2H++2e-=H2↑;有气泡产生.
点评:本题考查了原电池,明确正负极的判断方法及电极上发生的反应是解本题关键,根据电极反应确定发生的现象,题目难度不大.

练习册系列答案
相关题目
下列溶液中物质的量浓度为1mol/L的是( )
| A、将40 g NaOH溶解在1 L水中 |
| B、将22.4 L HCl气体溶于水配成1 L溶液 |
| C、将1 L 10 mol/L浓盐酸加入9 L水中 |
| D、将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL |
下列各试验中,不能产生气体的是( )
| A、红热的木炭投入浓硫酸中 |
| B、铜丝投入热的浓硫酸中 |
| C、铝片投入冷的浓硝酸中 |
| D、铁片投入热的浓硝酸中 |
反应4NH3(气)+5O2(气)?4NO(气)+6H2O(气)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.54mol,则此反应的平均速率
(X)(反应物的消耗速率或产物的生成速率)可表示为( )
. |
| v |
A、
| ||
B、
| ||
C、
| ||
D、
|
欲提高合成氨:N2+3H2?2NH3反应的反应速率,下列措施可行的是( )
①采用高温 ②采用高压 ③使用催化剂 ④增大N2的浓度 ⑤增大H2的浓度.
①采用高温 ②采用高压 ③使用催化剂 ④增大N2的浓度 ⑤增大H2的浓度.
| A、①②③ | B、②③④ |
| C、①③⑥ | D、全部 |
 利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个原电池(正极材料用碳棒).装置图
利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个原电池(正极材料用碳棒).装置图