题目内容
16.下列电子式错误的是( )| A. | 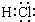 | B. | 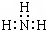 | C. | 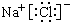 | D. |  |
分析 A.HCl为共价化合物,分子中存在1对共用电子对,氯原子最外层一个为8个电子.
B.NH3为共价化合物,分子中存在3对共用电子对,氮原子最外层为8个电子;
C.NaCl为离子化合物,电子式中需要标出阴阳离子所带电荷;
D.NaOH为离子化合物,含离子键和O-H共价键,由钠离子和氢氧根离子构成.
解答 解:A.HCl为共价化合物,分子中存在1对共用电子对,氯原子最外层一个为8个电子,电子式为 ,故A正确;
,故A正确;
B.NH3为共价化合物,分子中存在3对共用电子对,氮原子最外层为8个电子,电子式为 ,故B错误;
,故B错误;
C.NaCl为离子化合物,电子式中钠离子形成离子符号形式,氯离子需要标出最外层电子,电子式为 ,故C正确;
,故C正确;
D.NaOH为离子化合物,含离子键和O-H共价键,由钠离子和氢氧根离子构成,其电子式为 ,故D正确;
,故D正确;
故选B.
点评 本题考查了电子式的判断,该题基础性强,难易适中,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
相关题目
6.下列物质中,既可用浓H2SO4干燥,又可用碱石灰干燥的是( )
| A. | Cl2 | B. | O2 | C. | SO2 | D. | NH3 |
7.下列对化学反应的认识错误的是( )
| A. | 有化学键破坏的一定是化学反应 | B. | 会产生新的物质 | ||
| C. | 可能会引起物质状态的变化 | D. | 一定伴随着能量的变化 |
11.下列物质中,能用铝制容器贮运的是( )
| A. | 冷的稀盐酸 | B. | 冷的浓硫酸 | C. | 冷的稀硫酸 | D. | 冷的稀醋酸 |
1.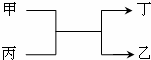 甲、乙为短周期同一主族元素的单质,丙、丁为氧化物,它们存在如图转化关系,下列各组的甲和乙一定符合的是( )
甲、乙为短周期同一主族元素的单质,丙、丁为氧化物,它们存在如图转化关系,下列各组的甲和乙一定符合的是( )
 甲、乙为短周期同一主族元素的单质,丙、丁为氧化物,它们存在如图转化关系,下列各组的甲和乙一定符合的是( )
甲、乙为短周期同一主族元素的单质,丙、丁为氧化物,它们存在如图转化关系,下列各组的甲和乙一定符合的是( )| A. | 钠和氢 | B. | 氧和硫 | C. | 碳和硅 | D. | 氟和氯 |
6.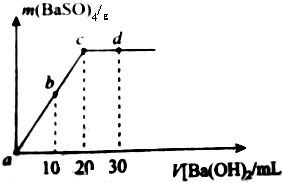 室温下,向20m1,物质的量浓度为0.35mol/L的H2SO4溶液中逐滴加人浓度的Ba(OH)2溶液,生成的沉淀与加人Ba(OH)2的体积如图(混合后体积变化忽略不计)下列说法不正确的是( )
室温下,向20m1,物质的量浓度为0.35mol/L的H2SO4溶液中逐滴加人浓度的Ba(OH)2溶液,生成的沉淀与加人Ba(OH)2的体积如图(混合后体积变化忽略不计)下列说法不正确的是( )
 室温下,向20m1,物质的量浓度为0.35mol/L的H2SO4溶液中逐滴加人浓度的Ba(OH)2溶液,生成的沉淀与加人Ba(OH)2的体积如图(混合后体积变化忽略不计)下列说法不正确的是( )
室温下,向20m1,物质的量浓度为0.35mol/L的H2SO4溶液中逐滴加人浓度的Ba(OH)2溶液,生成的沉淀与加人Ba(OH)2的体积如图(混合后体积变化忽略不计)下列说法不正确的是( )| A. | Ba(OH)2的物质的量浓密度为0.35mol/L | |
| B. | b时刻溶液中SO${\;}_{4}^{2-}$的浓度约为0.175mol/L | |
| C. | c时刻溶液显中性 | |
| D. | 实验过程中a、b、c三处溶液的导电能力c<b<a |