题目内容
下列四个反应可用H++OH-=H2O表示的是( )
| A、氨水与盐酸反应 |
| B、向醋酸溶液中加入适量NaOH溶液 |
| C、稀硫酸与Ba(OH)2溶液反应 |
| D、NaOH溶液与稀硫酸反应 |
考点:离子方程式的书写
专题:离子反应专题
分析:强酸与强碱反应生成可溶性盐和水的离子反应为H++OH-=H2O,以此来解答.
解答:
解:A.一水合氨为弱碱,在离子反应中保留化学式,不能用H++OH-=H2O表示,故A不选;
B.醋酸为弱酸,在离子反应中保留化学式,不能用H++OH-=H2O表示,故B不选;
C.反应生成硫酸钡沉淀和水,硫酸钡在离子反应中保留化学式,不能用H++OH-=H2O表示,故C不选;
D.反应生成硫酸钠和水,离子反应为H++OH-=H2O,故D选;
故选D.
B.醋酸为弱酸,在离子反应中保留化学式,不能用H++OH-=H2O表示,故B不选;
C.反应生成硫酸钡沉淀和水,硫酸钡在离子反应中保留化学式,不能用H++OH-=H2O表示,故C不选;
D.反应生成硫酸钠和水,离子反应为H++OH-=H2O,故D选;
故选D.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重中和反应的离子反应考查,注意在离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
| A、容量瓶中原有少量的蒸馏水 |
| B、定容时俯视刻度线和液面 |
| C、用适量蒸馏水洗涤烧杯和玻璃棒2-3次,洗涤液转移到容量瓶中 |
| D、移液时,不慎将液体流到瓶外 |
下列物质中,能导电且为电解质的是( )
| A、熔融态的NaC1 | B、固体NaOH |
| C、铁 | D、稀硫酸 |
目前市场上的手提应急灯,主要用的是“无液干粉”铅酸蓄电池,其原理是将强腐蚀性的浓硫酸灌注到硅胶中,使电解质溶液不易发生泄漏,大大改善了电池的性能.所用的原料仍然是Pb-PbO2-H2SO4,下列关于该铅酸蓄电池的说法正确的是( )
| A、充电时,电源的正极接蓄电池标“+”的一极,电池上标有“-”的一极发生氧化反应 |
| B、“无液干粉”铅酸蓄电池彻底改变了原来的铅酸蓄电池的原理 |
| C、放电时,在铅酸蓄电池的负极发生还原反应 |
| D、若用此铅酸蓄电池电解饱和NaCl溶液,标准状况下制备1.12LCl2,电池内至少消耗H2SO40.10 mol |
下列各组内两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A、氢氧化钠与硝酸;氢氧化钾与盐酸 |
| B、碳酸钠与硝酸;碳酸氢钠与盐酸 |
| C、硫酸与氢氧化钡;硫酸雨氯化钡 |
| D、硫酸铜与氢氧化钡;氯化铜与氢氧化钡 |
分析下列各物质的物理性质,可判断其固态不属于分子晶体的是( )
| A、碳化铝,黄色晶体,熔点2200℃.熔融态不导电 |
| B、溴化铝,无色晶体,熔点98℃,熔融态不导电 |
| C、五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、氯仿、丙铜中 |
| D、干冰,无色晶体,熔融时不导电 |
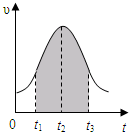 实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L?s)]与反应时间t(s)的关系如图所示.该反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L?s)]与反应时间t(s)的关系如图所示.该反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O